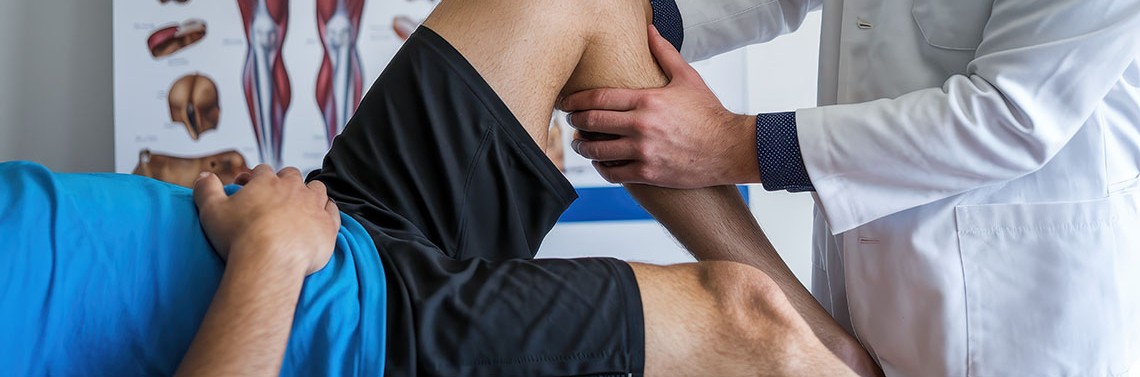
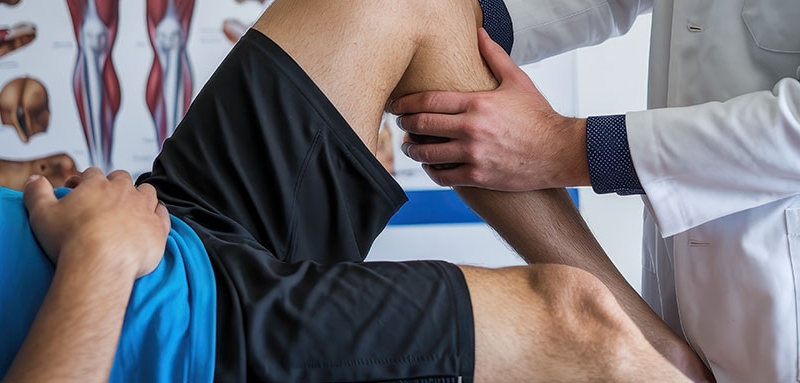
Jednym z najpoważniejszych problemów współczesnej medycyny jest walka z bólem. Szczególne trudności napotyka opanowanie tzw. bólu przewlekłego, jaki według kryteriów Komitetu Systematyki Międzynarodowego Towarzystwa Badania Bólu (ang. International Associastion for the Study of Pain – IASP) definiowany jest jako nieprzyjemne, subiektywne doznanie trwające powyżej trzech miesięcy, które towarzyszy istniejącemu lub zagrażającemu uszkodzeniu tkanek [1]. Wobec ograniczonej skuteczności farmakoterapii i poważnych ubocznych działań niepożądanych leków przeciwbólowych, a zwłaszcza opioidów, szczególnie w przypadku leczenia bólu neuropatycznego, istnieje wciąż rosnące zainteresowanie rozwojem technik miniinwazyjnych leczenia bólu środkami fizykalnymi – laser, stymulatory, kriolezja, termolezja. Techniki te stosowane są głównie przez specjalistów leczenia bólu, w szczególności przez anestezjologów, to jednak niektóre z nich mogą być cennym uzupełnieniem praktyki ortopedy.
REKLAMA
Kriolezja
Zabiegi z użyciem niskiej temperatury w celu łagodzenia bólu stosowano już od czasów starożytności. W czasach nowożytnych znane były sposoby zamrażania tkanki nowotworowej położonej powierzchownie (guzy szyi) aż do fazy jej martwicy z użyciem lodu i soli (J. Arnott 1797–1983), a w końcu XIX w. wprowadzono zastosowanie ciekłego azotu lub CO2 jako miejscowe leczenie zmian skórnych (White, Pusey, Whitehouse). Dopiero jednak w 1963 r. Cooper zaprojektował sondę do termicznego uszkodzenia tkanek (kriolezja, krioablacja), której konstrukcja przypomina współcześnie stosowane aplikatory do kriolezji. Dzięki zastosowaniu stałego przepływu ciekłego azotu w sondzie udało mu się uzyskać temperaturę chłodzenia –196°C [2, 3].
Obecnie stosowane sondy do kriolezji wykorzystujące zjawisko Joule’a-Thomsona mają dwa kanały różniące się średnicą, dzięki czemu gwałtowne rozprężanie gazu (CO2 lub NO) wydostającego się z przewodu o węższej średnicy „kradnie” ciepło z otoczenia, powodując spadek temperatury na końcówce sondy do ok. –70°C, co uwidacznia się w uwodnionej tkance jako powstająca kula lodu. Rozmiary pola chłodzenia zależą od średnicy sondy (obecnie na rynku od 1,2 do 2 mm), czasu mrożenia i stopnia ukrwienia (uwodnienia) tkanki.
Szybki efekt blokowania przewodzenia impulsów nerwowych w nerwie podobny jest do działania lokalnego leku znieczulającego (krioanalgezja), natomiast długotrwały efekt przypisywany jest mikrokryształom, jakie uszkadzają unaczynienie nerwu, doprowadzając do endoneuralnego obrzęku z następową martwicą Walerianowską przy zachowaniu jednak w całości osłonki mielinowej, co pozwala na regenerację nerwu po okresie od kilku do kilkunastu miesięcy [4].
Ze względu na czasowe wyłączenie przewodnictwa nerwowego kriolezja jest stosowana wyłącznie w zakresie unerwienia dróg czuciowych (wyjątek nerw nadłopatkowy), gdyż uszkodzenie nerwu ruchowego mogłoby spowodować nieodwracalne zmiany w efektorze mięśniowym do czasu jego reinerwacji. Kriolezja jest najskuteczniejsza w zespołach bólowych pochodzących z małych, dobrze określonych generatorów bólu – najczęściej lokalnych uszkodzeń nerwów obwodowych.
Oto główne wskazania do zastosowania kriolezji:
- ból czaszkowo-twarzowy – neuralgie gałęzi nerwu
- trójdzielnego, nerwów potylicznych większego i mniejszego, nerwu potylicznego trzeciego, nerwu językowo-gardłowego, nerwu usznego większego,
- ból klatki piersiowej po torakotomii, po złamaniach żeber, po półpaścu,
- ból ściany brzucha – neuralgie nerwu biodrowo-podbrzusznego, nerwu udowo-płciowego i nerwu biodrowo-pachwinowego,
- ból miednicy i krocza – neuralgia nerwu sromowego, nerwów pośladkowych, nerwów zasłonowych, staw krzyżowo-biodrowy, kokcygodynia,
- ból kręgosłupa pochodzenia stawowego (pseudokorzeniowy) – gałązki przyśrodkowe odchodzące od gałęzi grzbietowych nerwu rdzeniowego,
- ból kończyny górnej – neuralgia nerwu nadłopatkowego, gałązki okostnowe w rejonie entezopatii i zmian zwyrodnieniowo-wytwórczych, gałązka powierzchowna nerwu promieniowego, nerwiaki poamputacyjne,
- ból kończyny dolnej – neuralgia nerwu skórnego bocznego uda, nerwu udowo-goleniowego, gałązki okostnowe w rejonie entezopatii i zmian zwyrodnieniowo-wytwórczych, gałązki kolanowe nerwu piszczelowego, ostroga piętowa, nerwiak Mortona.
Technika zabiegu i opieka pozabiegowa
Kwalifikacja do zabiegu odbywa się po badaniu klinicznym, analizie badań obrazowych, ale przede wszystkim po pozytywnym wyniku iniekcji diagnostycznej w okolicy planowanej kriolezji z użyciem lokalnego anestetyku. Redukcja bólu o ponad 70% (nawet krótkotrwała) jest dobrym wskaźnikiem prognostycznym. Należy ułożyć pacjenta odpowiednio do topografii nerwu, który ma być celem zabiegu. Znieczulenie miejscowe skóry, wprowadzenie sondy mrożącej może nastąpić przez mininacięcie skóry lub torem kaniuli wenflonu, który pozwala na przeprowadzenie sondy mrożącej również przez barierę powięzi. Sonda mrożąca wprowadzana jest pod kontrolą USG lub RTG (ramię C) i tak kierowana, aby jej końcówka (czoło aktywne) znalazła się w bezpośrednim sąsiedztwie nerwu. Jeżeli aparat wyposażony jest w stymulację – położenie nerwu można potwierdzić stymulacją czuciową (100 Hz) i ruchową (2 Hz). Jeżeli podczas stymulacji czuciowej ból odczuwany przez pacjenta ma podobny charakter i topografię do bólu typowego dla pacjenta, uzyskuje się dodatkową informację diagnostyczną i pozytywny czynnik rokowniczy. Zazwyczaj przeprowadza się 2–3 cykle mrożenia trwającego 1–2 minuty z odstępem między cyklami 30–45 s pozwalającymi na odmrożenie sondy. Większość celów w zakresie nerwów obwodowych jest dobrze dostępna dla kontroli USG, pozwalając na bezpośrednie śledzenie powstającej kuli lodu. W zakresie kręgosłupa wystarczą kostne punkty odniesienia do lokalizacji gałązek stawowych, choć w obecności implantów lub nasilonych zmian zwyrodnieniowych i deformacji lokalizacja ich może być znacznie utrudniona lub wręcz niemożliwa (cień akustyczny). Zabieg może być wykonywany ambulatoryjnie. W czasie jednej sesji można zamrozić kilka punktów, w zależności od tolerancji pacjenta na ból, który związany jest początkowo ze stymulacją nerwu, a potem w początkowej fazie mrożenia z jego drażnieniem przez niską temperaturę. Jeżeli jest on nasilony, można porcjować czas mrożenia w cyklu lub podać lokalny lek znieczulający. Pacjent po 15 minutach obserwacji może udać się do domu samodzielnie.
W praktyce autora pierwsza kontrola po terapii wykonywana jest po dwóch miesiącach, do tego czasu pacjent proszony jest o zaniechanie czynności przeciążeniowych, łącznie ze sportami skokowo-biegowymi, pozostałe czynności wykonuje normalnie. Należy uprzedzić pacjenta, że nieznaczny dyskomfort związany z wkłuciami i stymulacją może utrzymywać się do trzech tygodni i w tym okresie można używać zwykłych leków przeciwzapalnych i przeciwbólowych (zdj. 1–3).
Tab. 1. Zestawienie lokalizacji kriolezji
Kriolezja – łącznie 175 zabiegów
- LS i SI – 118
- Kolano – 13 (zmiany wytwórcze i gałązki kolanowe)
- Stopa – 11 (ostroga piętowa, zmiany wytwórcze stawów, trzeszczka, inny nerwiak)
- Biodro – 9 (entezopatie okolicy krętarza i zmiany zwyrodnieniowe stawu)
- Th – 5
- C – 5
- Nerw nadłopatkowy – 4
- Morton – 3
- Entezopatia okolicy stawu łokciowego – 3
- Kikut – 1
- Nerw skórny boczny uda – 1
- Żebra – 1
- Bark – 1 (zmiany wytwórcze)
Tab. 2. Zestawienie lokalizacji termolezji
Termolezja (2015–2016) – łącznie 114 zabiegów
- LS i SI – 75
- Kolano – 9
- Nerw nadłopatkowy – 7
- Morton – 6
- C – 4
- Mięsień gruszkowaty – 3
- Nerw sromowy – 3
- Th – 2
- Biodro – 2
- Nerw biodrowo-podbrzuszny i biodrowo-pachwinowy – 2
- Żebra – 1
Przeciwwskazania do zabiegu
Przeciwwskazaniami do zabiegu są:
- brak współpracy z pacjentem (konieczny dobry kontakt w czasie stymulacji i mrożenia),
- ciężkie koagulopatie,
- zmiany infekcyjne skóry w rejonie planowanej kriolezji.
Termolezja
Zabieg o podobnym do kriolezji działaniu przeciwbólowym, tu jednak wykorzystuje się wysoką temperaturę 70–90°C uzyskaną na końcu specjalnej elektrody podłączonej do generatora prądu o bardzo wysokiej częstotliwości (500 kHz) – stąd alternatywna nazwa zabiegu radiofrekwencja (RF). Metodę można zastosować do termicznego uszkodzenia zakończeń nerwowych przewodzących ból poprzez ciągłą RF (ang. continous radiofrequency – CRF), gdzie temperatura osiąga powyżej 70°C lub do neuromodulacji, stosując temperaturę 42°C metodą pulsacyjną (ang. pulsed radiofrequency – PRF) poprzez odpowiednią modulację elektryczną w celu wyłączenia przewlekłego bólu spowodowanego aktualnym lub zastarzałym uszkodzeniem korzeni nerwowych i nerwów obwodowych [5].
Pierwsze generatory prądu wysokiej częstotliwości o zastosowaniu medycznym pojawiły się w latach 50. XX w. (B.J. Cosman, S. Aranow, O.A. Wyss). Do powszechnego użycia zabieg został wprowadzony w latach 60. w formie monopolarnej (pojedyncze pole ciepła wokół elektrody), a następnie w formie bipolarnej lub multipolarnej (pole ciepła między dwoma i więcej elektrodami). Idea zabiegu opiera się na polu przegrzania tkanki o promieniu ok. 3–4 mm od środka igły, więc potrzebna jest bardzo precyzyjna lokalizacja igły poprzez stymulację czuciową i ruchową. Termolezja ma tę przewagę nad kriolezją, że może być wykonywana wielopunktowo (nawet kilkanaście punktów bólowych), bowiem igła zabiegowa ma bardzo niewielką średnicę, a przy technice multipolarnej obszar lezji obejmuje znaczną powierzchnię między aktywnymi elektrodami i może być zastosowana np. w okolicy stawu krzyżowo-biodrowego (tzw. technika palisadowa). Zabieg daje znacznie większe możliwości neuromodulacji bólu niż kriolezja, gdyż może być stosowany w formie pulsacyjnej, sięgając temperatury 42°C w takich wskazaniach, jak zespoły usidlenia nerwów obwodowych, zbliznowacenia wewnętrzne nerwów i korzeni po niepowodzeniach leczenia operacyjnego, a nawet w zakresie modulacji napięcia mięśni (zespół mięśnia gruszkowatego) czy dezaktywacji punktów spustowych w bólu powięziowym. Mechanizm neurodestrukcji jest nieco inny niż w przypadku zabiegu kriolezji. Dochodzi wprawdzie również do degeneracji Walerianowskiej we wszystkich włóknach nerwowych, ale również do rozerwania błony podstawnej, lokalnego uszkodzenia perineurium, degranulacji komórek tucznych, a także uszkodzenia osłonki mielinowej ze znaczną aktywacją makrofagów zaangażowanych w „sprzątanie” lokalnej martwicy. Stąd teoretycznie dłuższy okres odnerwienia niż w przypadku kriolezji, ale również wyższy poziom odpowiedzi autoimmunologicznej i związane z nią potencjalne kłopoty (dolegliwości bólowe o typie neuritis). Mechanizm neuromodulacji zabiegiem PRF nie został do końca wyjaśniony – najczęściej cytowana jest hipoteza wpływu szybkich zmian pola elektromagnetycznego powodująca desensytyzację nerwu obwodowego, rdzenia lub zwoju grzbietowego nerwu rdzeniowego w zależności od miejsca aplikacji [6, 7].
W doniesieniach odnoszących się do skuteczności termolezji średnia skuteczność zabiegu mierzona stopniem redukcji bólu oscyluje na poziomie 50–60% w perspektywie kilku do kilkunastu miesięcy, przy czym nie wykazano wyraźnego związku między redukcją bólu, czasem jego trwania, poziomem stymulacji czy poziomem leczonego segmentu. Wykazano jednak dłuższe utrzymywanie się efektu przeciwbólowego w przypadku zabiegów lezji RF niż zabiegów PRF [8–10].
Główne wskazania do zastosowania termolezji i termomodulacji
Głównymi wskazaniami do zastosowania termolezji i termomodulacji są:
- ból czaszkowo-twarzowy – zwój klinowo-podniebienny, zwoje współczulne szyjne, neuralgie gałęzi nerwu trójdzielnego, nerwów potylicznych większego i mniejszego, nerwu potylicznego trzeciego, nerwu językowo-gardłowego, nerwu usznego większego,
- ból klatki piersiowej po torakotomii, po złamaniach żeber, po półpaścu,
- ból ściany brzucha – neuralgie nerwu biodrowo-podbrzusznego, nerwu udowo-płciowego i nerwu biodrowo-pachwinowego,
- ból miednicy i krocza – neuralgia nerwu sromowego, nerwów pośladkowych, nerwów zasłonowych, staw krzyżowo-biodrowy, kokcygodynia, zwój nieparzysty (zwój Walthera),
- ból kręgosłupa pochodzenia stawowego (pseudokorzeniowy) – gałązki przyśrodkowe odchodzące od gałęzi grzbietowych nerwu rdzeniowego,
- ból korzeniowy i zwoju grzbietowego nerwu rdzeniowego – PRF,
- ból kończyny górnej – neuralgia nerwu nadłopatkowego, zespoły usidlenia nerwów obwodowych, gałązki okostnowe w rejonie entezopatii i zmian zwyrodnieniowo-wytwórczych,
- ból kończyny dolnej – neuralgia nerwu skórnego bocznego uda, nerwu udowo-goleniowego, zespoły usidlenia nerwów obwodowych, gałązki okostnowe w rejonie entezopatii i zmian zwyrodnieniowo-wytwórczych, gałązki kolanowe nerwu piszczelowego, nerwiak Mortona.
Technika zabiegu i opieka pozabiegowa
Kwalifikacja do zabiegu odbywa się podobnie jak w przypadku kriolezji – bardzo ważna jest iniekcja diagnostyczna potwierdzająca generator bólu będący celem zabiegu. Należy ułożyć pacjenta odpowiednio do topografii nerwu, który ma być celem zabiegu. Trzeba nakleić elektrodę uziemiającą i podłączyć ją do generatora. Nie jest konieczne znieczulenie skóry, gdyż elektroda jest średnicy cienkiej igły i nakłucie kaniulą jest zupełnie dobrze tolerowane. Kaniula jest wprowadzana pod kontrolą USG lub RTG. Elektroda aktywna jest wprowadzana przez kaniulę po usunięciu rdzenia. Stymulacja czuciowa i ruchowa potwierdza położenie elektrody. Jeżeli wykonuje się termolezję, podczas stymulacji ruchowej nie może być nawet śladu odpowiedzi ruchowej w mięśniach kończyny, w przeciwnym razie zakres lezji zagraża nieodwracalnym uszkodzeniem włókien ruchowych korzenia. Następnie torem kaniuli po usunięciu elektrody wprowadza się lokalne znieczulenie – lignokaina 1–2% i po dwuminutowej przerwie rozpoczyna się zabieg. Czas lezji to zazwyczaj 1,5 minuty na punkt, w miejsce lezji można podać niewielką porcję leku sterydowego, zapobiegając pozabiegowym dolegliwościom związanym z mikrooparzeniem. Jeżeli celem zabiegu jest neuromodulacja, położenie nerwu można potwierdzić stymulacją czuciową i ruchową, a następnie zastosować PRF 42°C w 2–3 cyklach czterominutowych. Wadą zabiegu jest to, że po PRF, którego właściwie pacjent nie czuje podczas zabiegu, nie można przewidzieć jego wyniku do chwili kontroli po kilku lub kilkunastu tygodniach, co może być frustrujące dla pacjenta opuszczającego klinikę. Jeżeli podczas stymulacji czuciowej ból odczuwany przez pacjenta ma podobny charakter do tego, jaki trapi go na co dzień, uzyskuje się dodatkową informację diagnostyczną i pozytywny czynnik rokowniczy. Podobnie jak w przypadku kriolezji większość celów dla termolezji w zakresie nerwów obwodowych i punktów przebiegu gałązek stawowych kręgosłupa jest dobrze dostępna dla kontroli USG, chociaż zastrzeżenia lokalizacji gałązek stawowych są podobne jak w przypadku kriolezji (implanty, nasilone zmiany zwyrodnieniowe). Zabieg może być wykonywany ambulatoryjnie. W czasie jednej sesji można wykonać termolezję nawet kilkunastu punktów ze względu na atraumatyczną technikę zabiegu. Pacjent po 15 minutach obserwacji może udać się do domu samodzielnie. Podobnie jak w przypadku zabiegów kriolezji, w praktyce autora pierwsza kontrola po terapii wykonywana jest po dwóch miesiącach, do tego czasu pacjent proszony jest o zaniechanie czynności przeciążeniowych, łącznie ze sportami skokowo-biegowymi, pozostałe czynności wykonuje normalnie. Należy uprzedzić pacjenta, że nieznaczny dyskomfort związany z wkłuciami i stymulacją może utrzymywać się do trzech tygodni i w tym okresie można używać zwykłych leków przeciwzapalnych i przeciwbólowych (zdj. 4–6).
Przeciwwskazania do zabiegu
Przeciwwskazaniami do zabiegu są:
- brak współpracy z pacjentem (konieczny dobry kontakt w czasie stymulacji i lezji),
- ciężkie koagulopatie,
- zmiany infekcyjne skóry w rejonie planowanej termolezji,
- stymulator serca (względne przeciwwskazanie).
Materiał własny
W latach 2011–2016 przeprowadzono łącznie 289 zabiegów miniinwazyjnego leczenia zespołów bólowych. Wykonano 175 zabiegów kriolezji u 169 osób (u niektórych pacjentów zabiegi były powtarzane lub wykonywane w kilku lokalizacjach), w tym 128 kobiet i 41 mężczyzn, mediana wieku to 63,32, oraz 123 zabiegi termolezji u 120 osób, w tym 76 kobiet i 44 mężczyzn, mediana wieku to 68,45. Procentowy udział lokalizacji przedstawiają tabela 1 (kriolezja) i tabela 2 (termolezja) (tab. 1 i 2).
Wszystkie zabiegi były przeprowadzone pod kontrolą USG w znieczuleniu miejscowym w warunkach ambulatoryjnych. Kontrolę po zabiegu przeprowadzano po dwóch miesiącach.
Do oceny skuteczności zabiegu zastosowano w obu technikach kwestionariusz SMC – Sutherland Medical Center (modyfikacja skali Likerta) zawierający trzy pytania oceniające: redukcję wyjściowego bólu, poprawę dominującej funkcji i stosunek ceny zabiegu do odniesionego zysku (zabiegi były wykonywane wyłącznie komercyjnie), przyporządkowując punktację według poniższego wzoru.
Redukcja wyjściowego bólu:
- bez zmiany – 0 pkt,
- nieznaczna poprawa, ból nadal dokuczliwy – 1 pkt,
- wyraźna poprawa, ale pozostał resztkowy ból – 2 pkt,
- zupełne ustąpienie bólu – 3 pkt.
Poprawa dominującej funkcji dotychczas niedostępnej lub znacznie ograniczonej – subiektywnie wybranej przez pacjenta (chodzenie, siedzenie, jazda samochodem, praca biurowa, spanie, sport itp.):
- bez zmiany – 0 pkt,
- nieznaczna poprawa, nadal funkcja znacznie ograniczona – 1 pkt,
- wyraźna poprawa, funkcja podjęta, ale pozostał resztkowy dyskomfort podczas jej podejmowania – 2 pkt,
- pełny powrót do funkcji – 3 pkt.
Poziom satysfakcji, biorąc pod uwagę stosunek ceny zabiegu do zysku, jaki odniósł pacjent – czy poleciłbyś przyjacielowi lub członkowi rodziny ten zabieg, biorąc pod uwagę stosunek kosztów do zysku?
- z pewnością nie – 0 pkt,
- raczej nie – 1 pkt,
- raczej tak – 2 pkt,
- z pewnością tak – 3 pkt.
Suma punktów określa ocenę globalnej satysfakcji pacjenta: 9 pkt = 100%.
Tab. 3. Porównanie metod
| Kriolezja | Termolezja | |
| Zalety |
|
|
| Wady |
|
|
Wyniki
Kontrola po zabiegach kriolezji objęła 125 osób – oto wyniki dla największej grupy pacjentów (kręgosłupa LS) –
81 przypadków:
![]()
Kontrola po zabiegach termolezji objęła 86 osób – oto wyniki dla największej grupy pacjentów (kręgosłupa LS) –
59 przypadków:
![]()
Omówienie wyników i dyskusja
Grupa pacjentów z zespołami bólowymi odcinka lędźwiowego była w analizowanym materiale szczególnie niehomogenna pod względem lokalizacji generatora bólu – kwalifikowane były przypadki nie tylko z komponentą bólu stawowego (podstawowe wskazanie), ale również pacjenci z komponentą bólu wynikającą z niestabilności kręgosłupa (kręgozmyk, znaczne zaburzenia osi) i stenozy kanału kręgowego, a nawet pacjenci z zespołami bólowymi po złamaniu osteoporotycznym kręgu czy leczeniu operacyjnym. U wielu z nich zespół bólowy kręgosłupa lędźwiowego nakładał się na bóle wynikające ze zmian zwyrodnieniowych stawu biodrowego i kolana oraz zespoły bólu mięśniowo-powięziowego. W ogromnej większości dolegliwości trwały powyżej trzech miesięcy, a często nawet wiele lat, mimo rehabilitacji i opieki farmakologicznej. Nie zaobserwowano żadnej wyraźnej korelacji między czasem trwania bólu, zaawansowaniem procesu zwyrodnieniowego a poziomem satysfakcji. Zdarzały się tak graniczne przypadki kwalifikowane do procedury, jak stenoza kanału kręgowego z wyraźną poprawą subiektywną po wykonaniu procedury, a z drugiej strony przypadki typowych zmian stawowych, które mimo – wydawałoby się – najlepszego dopasowania do procedury nie przynosiły satysfakcjonujących wyników. Stąd być może biorą się paradoksalne oceny termolezji w piśmiennictwie.
Termolezja jest metodą znaną i szeroko używaną w klinikach leczenia bólu na całym świecie od kilku dekad, a mimo to we wnioskach przeglądu piśmiennictwa z roku 2015 dotyczącego leczenia zespołów bólowych odcinka lędźwiowego z zastosowaniem RF, gdzie prześledzono 23 badania z randomizacją, które objęły łącznie 1309 pacjentów, znalazł się zapis o braku wysokiej jakości dowodów na to, że zabiegi RF redukują ból i poprawiają funkcje [11].
Mimo to w poszczególnych doniesieniach oceniających efektywność termolezji w tzw. globalnym odczuwalnym efekcie (ang. global perceived effect – GPE) zawierający skalę VAS (ang. visual analogue scale) i kwestionariusze punktowe będące modyfikacją skali Likerta, podobnie jak zastosowany kwestionariusz SMC (np. czteropunktowe – całkowite ustąpienie bólu, ponad 50-procentowe ustąpienie bólu, brak efektu, pogorszenie bólu) lub Oswestry Index oscylują na poziomie 39–60%, przy czym należy przyznać, że nawet tzw. udawana terapia (ang. sham therapy) okazuje się sięgać efektywnością 27% [12–15].
Jeśli zaś chodzi o kriolezję, doniesień o jej efektywności potwierdzonej w prospektywnych badaniach z randomizacją jest znacznie mniej. W badaniu z 2007 r. Birkenmaiera, gdzie dokonano prospektywnej oceny 50 pacjentów poddanych kriolezji odcinka LS pod względem skali VAS, kwestionariusza aktywności McNaba i ogólnej satysfakcji, po sześciu tygodniach 72% pacjentów raportowało ustąpienie lub znaczne złagodzenie bólu, jednak po roku odsetek ten spadł do 57% [14].
Podsumowanie
Jak widać z powyższej tabeli, obie metody mają swoje wady i zalety. Zacznijmy od kriolezji. Metoda jest bardzo skuteczna przy dokładnej lokalizacji gałązki bólowej. Już w czasie zabiegu dochodzi do płenego wyeliminowania bólu, co daje bardzo dobry sygnał rokowniczy zarówno dla pacjenta, jak i wykonującego zabieg lekarza. Innymi słowy, wiadomo, czego się spodziewać, a jak widać z analizy materiału własnego, skuteczność kriolezji góruje nad tą uzyskaną zabiegami termolezji przy zastosowaniu tego samego algorytmu oceny. Oczywiście jest to zabieg znacznie bardziej traumatyzujący niż termolezja ze względu na średnicę sondy, a zaplanowanie więcej niż 5–6 punktów do mrożenia w jednej sesji może być problematyczne, zwłaszcza u osób w podeszłym wieku i we wrażliwej strefie (np. odcinek szyjny). Z drugiej jednak strony bardzo rzadko obserwuje się nasilenie dolegliwości po kriolezji, nawet jeżeli pacjent i lekarz spodziewali się więcej po zabiegu, to nie ma nieprzyjemnej sytuacji pogorszenia stanu wyjściowego. Niewielką wadą w porównaniu z termolezją jest to, że podczas całego cyklu mrożenia trzeba utrzymywać nieruchomo sondę mrożącą ze względu na jej rozmiary i połączenie z dość masywnym przewodem doprowadzającym gaz z aparatu do kriolezji, podczas gdy w przypadku termolezji po aplikacji elektrody we właściwe miejsce operator nie musi jej stale podtrzymywać, a po zaprogramowaniu parametrów na generatorze RF – zabieg „wykonuje się sam”. Na korzyść kriolezji przemawiają na pewno niższe koszty zakupu aparatu (w niektórych przypadkach dwukrotnie), a także stosunkowo małe koszty eksploatacyjne – zużycie gazu, sterylizacja sond itp.
Porównując obie metody, trzeba zauważyć znacznie większe możliwości zabiegowe termolezji i termomodulacji – posiada bowiem oprócz możliwości uszkodzenia gałązek nerwowych (lezji) – możliwości neuromodulacji nerwów obwodowych, terapię tkanek miękkich, a nawet procedury wewnątrzstawowe (choć trzeba przyznać uczciwie o nie do końca jeszcze ocenionej w piśmiennictwie skuteczności). Termolezja jest zabiegiem znacznie mniej traumatycznym – cienkie igły można aplikować praktycznie bezkrwawo, co powoduje, że w ciągu jednej sesji można wykonać nawet kilkanaście punktów (np. obustronną termolezję kręgosłupa lędźwiowego i stawów krzyżowo-biodrowych), co byłoby niewykonalne w przypadku kriolezji. W trakcie samego zabiegu jest możliwość nie tylko pełnego znieczulenia miejsca lezji poprzez kaniulę wprowadzającą igłę do termolezji, ale również płynnej modyfikacji temperatury na końcówce igły, stąd zabieg może być dostosowany do osobniczej tolerancji pacjenta na ból. A jednak nierzadko zdarzają się zespoły bólowe i nieprzyjemne, nie zawsze bólowe odczucia pacjenta (np. parestezje) i bóle deaferencyjne (ang. deafferentation pain syndrom), po wydawałoby się perfekcyjnym technicznie wykonaniu (niska stymulacja potwierdzająca lokalizację gałązki, pojedyncze wkłucie, atraumatyczna technika) [15].
Dodatkową wadą są wysokie koszty samego aparatu oraz w przypadku użycia zestawów jednorazowych – wysokie koszty eksploatacyjne (sonda, kaniula, elektroda uziemiająca).
Reasumując, kriolezja wydaje się idealnym rozwiązaniem dla terapii przewlekłego bólu kręgosłupa pochodzenia stawowego (łącznie ze stawem krzyżowo-biodrowym) przy stosunkowo niewielkiej liczbie punktów generujących ból. W zakresie nerwów obwodowych, zwojów współczulnych i terapii tkanek miękkich przewaga radiofrekwencji w wersji PRF wydaje się niepodważalna. Biorąc pod uwagę powyższe uwagi, można powiedzieć, że do zapewnienia pełnego spektrum miniinwazyjnej terapii bólu warto dysponować obydwoma sprzętami.