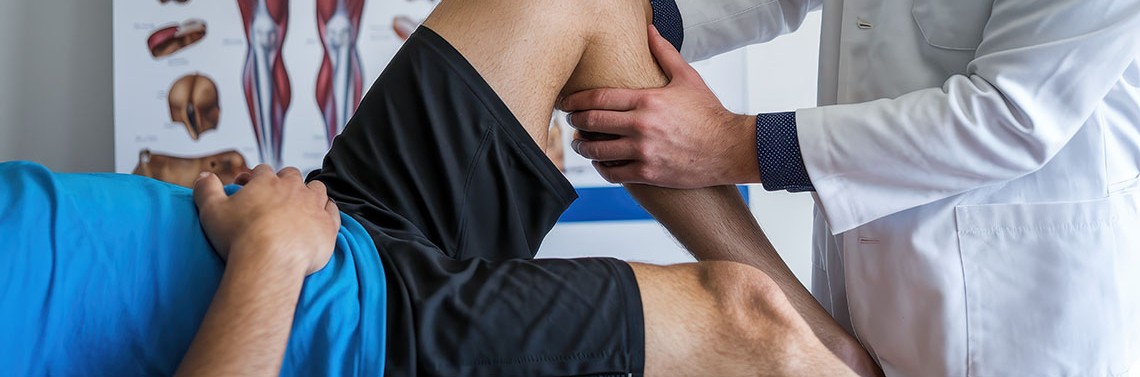
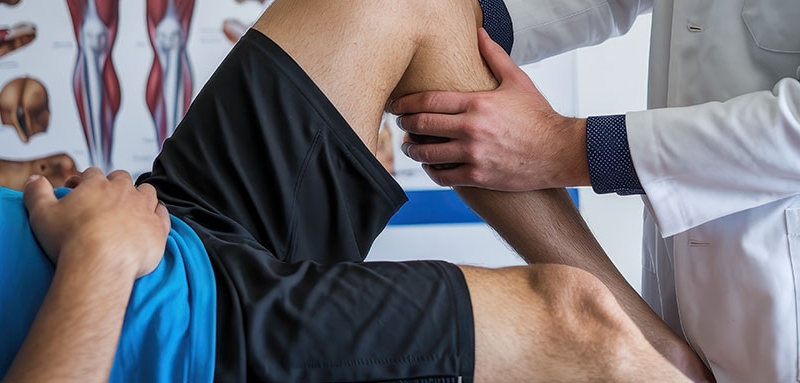
Choroba zwyrodnieniowa stawów jest zespołem o etiologii wieloczynnikowej, w którego następstwie dochodzi do zaburzeń równowagi w tworzeniu i niszczeniu chrząstki stawowej oraz degradacji wszystkich elementów stawu. Szacuje się, że w Polsce dotyczy 20–30% populacji powyżej 40. roku życia i jest jedną z głównych przyczyn kalectwa w wieku późniejszym. W leczeniu zachowawczym stosuje się głównie niesteroidowe leki przeciwzapalne (NLPZ), fizykoterapię oraz wiskosuplementację. W latach ostatnich lat nastąpił znaczący rozwój w zastosowaniu czynników autogennych, takich jak osocze bogatopłytkowe czy komórki macierzyste. Kwas hialuronowy jest szeroko stosowany i zalecany właśnie jako wiskosuplementacja w zmianach zwyrodnieniowych zarówno idiopatycznych, jak i pochodzenia reumatoidalnego, zapalnego czy pourazowych. Odpowiada on za elastyczność tkanki łącznej i właściwości wiskoelastyczne płynu stawowego. Zaobserwowano, że wykazuje również działanie przeciwbólowe, przeciwzapalne oraz chondroprotekcyjne.
REKLAMA
Kwas hialuronowy w budowie powierzchni stawowej
Powierzchnię stawową pokrywa chrząstka szklista, składająca się z pięciu warstw: powierzchniowej, pośredniej, promienistej (głębokiej), wapniejącej oraz podchrzęstnej.
Jej najbardziej zewnętrzną częścią jest warstwa powierzchniowa, leżąca w bezpośrednim sąsiedztwie jamy stawu. Pozbawiona jest komórek, za to zawiera liczne, ułożone równolegle do powierzchni stawowej, włókna kolagenu (typ II, IX i XI), mało glikozaminoglikanów i jest bogata w kwas hialuronowy. Warstwa powierzchniowa, stanowiąca ok. 10% grubości chrząstki, pełni funkcję błony ochronnej dla niżej leżących struktur chrzęstnych. W kolej warstwie, budującej 40% objętości chrząstki, włókna kolagenowe ułożone są skośnie. Dwie najgłębsze warstwy, stanowiące 50% grubości chrząstki, to warstwa promienista o prostopadłym przebiegu włókien kolagenu i warstwa zwapniała chrząstki, bezpośrednio stykająca się z warstwą podchrzęstną kości. Ten złożony, warstwowy układ włókien kolagenowych zapewnia chrząstce stawowej odpowiednią wytrzymałość i skuteczne rozpraszanie sił działających na staw w trakcie poruszania się ciała, a tym samym efektywną amortyzację i ochronę aparatu ruchu przed uszkodzeniem. Molekularnie strukturalną podstawę chrząstki stanowią agregaty proteoglikanu (agrekany), które w głównej mierze tworzone są przez różne glikozaminoglikany (GAG; siarczan chondroityny, dermatanu, keratanu, heparanu) połączone z innym ich rodzajem, czyli kwasem hialuronowym, który w odróżnieniu od pozostałych nie jest siarczanem. Wzajemne proporcje wspomnianych związków zmieniają się wraz z wiekiem, co może też stanowić podstawę diagnostyczną stopnia uszkodzenia struktur chrząstki stawowej. Cząsteczka agrekanu składa się z białka stanowiącego rdzeń cząsteczki, do którego poprzez specyficzne białka przyłączonych jest ok. 100 łańcuchów siarczanu chondroityny i w wielu przypadkach taka sama ilość ułożonych za nimi łańcuchów siarczanu keratanu. Cały kompleks jest dużą makromolekułą, o wielkości ok. 100 MDa, wykazującą ogromne zróżnicowanie zarówno w rozmiarze, jak i składzie. Koniec białka tworzącego rdzeń proteoglikanu, za pomocą specyficznych białek, połączony jest z długimi nićmi kwasu hialuronowego (ok. 100 białek rdzeniowych na jeden łańcuch kwasu hialuronowego).
Chondrocyty (komórki chrzęstne) stanowią tylko ok. 1% objętości chrząstki i są odpowiedzialne za syntezę, katabolizm i ogólną homeostazę chrząstki. Pozostają zawieszone w macierzy, która składa się głównie z wody (60–80% całej masy), kolagenu (60% suchej masy) i proteoglikanów (30% suchej masy). Fizjologia chrząstki i jej charakterystyczne, lepko-elastyczne (wiskoelastyczne) właściwości bezpośrednio wynikają z faktu, że to właśnie woda jest jej głównym składnikiem.. Przeciętnie grubość chrząstki waha się w granicach 0,5–2 mm; najgrubsza występuje na powierzchni stawowej rzepki, gdzie dochodzi do 6 mm. Ze względu na to, że u dorosłych chrząstka stawowa nie ma zakończeń nerwowych ani naczyń krwionośnych, jej zdolności regeneracyjne są ograniczone. Odżywiana jest drogą dyfuzji poprzez płyn stawowy, w skład którego wchodzą kwas hialuronowy, lubrycyna, proteinazy i kolagenzy. Wydzielany jest on przez komórki błony maziowej i tworzy na jej powierzchni warstwę o grubości ok. 50 µm. Najważniejszą funkcją płynu stawowego jest zmniejszenie tarcia pomiędzy powierzchniami chrząstek stawowych. Polisacharydowa budowa kwasu hialuronowego zapewnia, dzięki oddziaływaniom cukier – cukier i/lub cukier – białko, utworzenie lepkiej bariery na powierzchni chrząstki, skutecznie zapobiegającej jej degradacji, poprzez minimalizację uwalniania z zewnątrzkomórkowej macierzy proteoglikanów. Polisacharyd, jakim jest siarczan chondroityny (SC), stanowi podstawowy składnik macierzy zewnątrzkomórkowej wszystkich tkanek łącznych. Jego główną funkcją jest tworzenie proteoglikanów poprzez kowalencyjne połączenie z białkami. Podstawową cegiełkę strukturalną (monomer) chrząstkowego polisacharydu, jakim jest siarczan chondroityny, tworzy disacharyd, w skład którego wchodzi cząsteczka kwasu D-glukuronowego połączona wiązaniem 1,3 z cząsteczką N-acetyl-D-galaktozaminy. Monomery te są z kolei połączone ze sobą wiązaniem 1,4.

Polisacharydowe łańcuchy GAG po syntezie poddawane są modyfikacjom, poprzez przyłączenie do cząsteczki galaktozaminy grup sulfonowych w pozycji 4 albo 6. Zjonizowane grupy sulfonowe wraz z grupami karboksylowymi nadają łańcuchowi GAG ładunek ujemny.
Wzór rozmieszczenia grup sulfonowych w monomerach chondroityny jest różny w stawowej chrząstce ludzkiej, w zależności od wieku i obszaru chrząstki.
Powierzchnia stawowa tylko pozornie jest gładka, w rzeczywistości ma bardzo złożoną strukturę, na którą składają się liczne pofałdowania, drobniejsze zagłębienia i jeszcze niższego rzędu grzebienie. Dzięki takiej budowie powierzchnia chrząstki stawowej może osiągać bar-
dzo niski współczynnik tarcia, który waha się w zakresie 0,01–0,02 (dla kolana wynosi tylko 0,002). Współczynnik ten jest odwrotnie proporcjonalny do wzrostu obciążenia i znacząco zmniejsza się w wyniku pokrycia powierzchni stawu mazią stawową. Biomechaniczne właściwości chrząstki stawowej wynikają głównie z fizykochemicznych właściwości glikozaminoglikanów, stanowiących 80–90% masy proteoglikanów. Obecność szeregowo ułożonych grup hydroksylowych, zjonizowanych sulfonowych i karboksylowych powoduje przyciąganie do proteoglikanów, w wyniku pojawienia się sił elektrostatycznych, dużej liczby cząsteczek wody. Dipole wody pod wpływem nagromadzenia ładunków ujemnych organizują się w wielowarstwowe układy otaczające przyciągające je ładunki. Prowadzi to do powstania gradientów osmotycznych i indukcji wewnętrznego ciśnienia obrzmienia (swelling pressure). Kiedy chrząstka stawowa jest poddawana obciążeniu, związana elektrostatycznie woda jest wyciskana spomiędzy struktur proteoglikanów. Zbliżające się w następstwie tego do siebie ujemnie naładowane grupy powodują dalszy wzrost ciśnienia, dodatkowo utwardzając chrząstkę. Kiedy ucisk mija, dipole wody wracają do otoczenia ładunków ujemnych, odtwarzając uporządkowaną strukturę chrząstki.
Mechanizmy rozwoju stanu zwyrodnieniowego
Jeden z najczęściej proponowanych mechanizmów rozwoju stanu zwyrodnieniowego chrząstki stawowej jako główną jego przyczynę podaje wysoką dynamikę bodźca mechanicznego, który jest bardzo silny i działa krótko. Jego uszkadzający wpływ wynika z tego, że chrząstka stawowa i leżące pod nią warstwy wymagają czasu, aby dostosować kształt do raptownie zmieniających się warunków mechanicznych. Przy zbyt silnym bodźcu mechanizm ten nie może zadziałać i misterna struktura, oparta na koncepcji „materaca wypełnionego wodą”, może ulec uszkodzeniu i stracić swe hydrodynamiczne właściwości. W ten sposób może się rozpocząć proces depolimeryzacji proteoglikanów i degradacji chrząstki stawowej. W tabeli 1 podano klasyfikacje uszkodzeń chrząstki.
Etiologia choroby zwyrodnieniowej nie jest jednoznacznie wyjaśniona; podkreśla się wieloczynnikowe podłoże, gdzie istotne znaczenie mają zarówno czynniki genetyczne (gen COL2A1 odpowiedzialny za degradację kolagenu), jak i komponent zapalny, co potwierdza zwiększone stężenie interleukin (IL-1, IL-6, IL-8) w chrząstce stawowej. Poza tym znaczącą rolę w rozwoju zmian zwyrodnieniowych odgrywają liczne enzymy. Macierz chrząstki szklistej jest niszczona przez metaloproteinazy oraz dezintegrynę i trombospondynę. Kolagen rozkładany jest przez kolagenazy MMP-1 i MMP-13 oraz stromelyzynę (MMP-3), natomiast agrekany przez agrekanazy (ADAMTS).
Wymienione enzymy są indukowane przez czynniki prozapalne, takie jak interleukiny (zwłaszcza IL-1) i czynnik martwicy nowotworów α (tumor necrosis factor α – TNF-α). Wystawiona na działanie enzymów chrząstka zaczyna tracić kwas hialuronowy, co objawia się utratą jej właściwości mechanicznych oraz oznacza stopniową degradację. Badania wykazały, że kwas hialuronowy jest jednym z głównych czynników przeciwdziałających katabolicznemu działaniu IL-1 na chrząstkę stawową, hamuje również działanie TNF-α, wywiera bezpośredni wpływ nie tylko na chondrocyty, lecz także na fibroblasty błony maziowej.
| Klasyfikacja ICRS (International Cartilage Repair Society) |
Klasyfikacja Outerbridge | Klasyfikacja Noyesa |
| 0° Chrząstka prawidłowa |
||
|
I° |
I° Rozmiękanie i obrzęk chrząstki |
I° Powierzchnia chrząstki nienaruszona: IA – chrząstka miękka, bez trwałych zniekształceń IB – zniekształcenie chrząstki |
| II° Uszkodzenie niewielkie; defekt obejmuje < 50% grubości chrząstki |
II° Pęknięcia i ubytki < 0,5 cm średnicy |
IIA° Powierzchnia chrząstki uszkodzona – pęknięcia, ubytki, nieprzekraczające połowy grubości chrząstki |
| III° Uszkodzenie głębokie; defekt obejmuje > 50% grubości chrząstki |
III° Pęknięcia i ubytki > 0,5 cm średnicy, ale nieprzekraczające warstwy podchrzęstnej |
IIB° Powierzchnia chrząstki uszkodzona – pęknięcia, ubytki przekraczające połowy grubości chrząstki |
| IV° Uszkodzenie bardzo głębokie, sięgające do warstwy podchrzęstnej |
IV° Ubytki chrząstki przekraczające warstwę podchrzęstną |
III° Uszkodzenie chrząstki pełnej grubości, odsłonięcie kości gąbczastej IIIA – kość nieuszkodzona IIIB – geody w obrębie kości |
W przebiegu fibrynolizy, która jest jednym z głównych procesów powodujących zmiany zwyrodnieniowe, zasadniczą rolę odgrywa plazminogen. W stawach zdrowych zachowana jest równowaga pomiędzy działaniem aktywatora plazminogenu (PA) a inhibitorem aktywatora plazminogenu (PAI). Kwas hialuronowy jest czynnikiem modulującym aktywność układu PA–PAI w obrębie fibroblastów błony maziowej, co prowadzi do spowolnienia fibrynolizy aktywowanej plazminogenem.
Działanie kwasu hialuronowego w chorobie zwyrodnieniowej stawów
Niesteroidowe leki przeciwzapalne są głównym „narzędziem” w leczeniu choroby zwyrodnieniowej stawów. Działają poprzez hamowanie cyklooksygenazy (COX), co prowadzi do supresji prostaglandyn oraz leukoterienów w tkankach objętych procesem zapalnym. Liczne badania in vitro wykazały, że kwas hialuronowy ma różny wpływ na aktywność COX-2, w zależności od rodzaju komórek organizmu oraz od masy cząsteczkowej hialuronianu; wydaje się, że zdolność hamowania COX wykazują izoformy hialuronianu o dużej masie cząsteczkowej.
Dokładne wyjaśnienie mechanizmu korzystnego działania kwasu hialuronowego w chorobie zwyrodnieniowej stawów wymaga jeszcze dalszych badań, aczkolwiek na obecnym etapie dowiedziono, że efekt terapeutyczny jest skutkiem nie tylko poprawy wiskoelastyczności płynu stawowego i warunków biomechanicznych w obrębie stawu oraz lepszego uwodnienia chrząstki stawowej, lecz także wielotorowego działania przeciwzapalnego. Kwas hialuronowy, jako integralny składnik chrząstki stawowej, płynu stawowego oraz tkanki łącznej, zapewnia prawidłową strukturę, właściwości biomechaniczne i fizykochemiczne w obrębie stawów. W świetle przedstawionych informacji stosowanie iniekcji kwasu hialuronowego jest wysoce zasadne nie tylko we wczesnej fazie choroby zwyrodnieniowej, ale i na etapach późniejszych. Istnieją także doniesienia, że skuteczność takiej terapii jest porównywalna z iniekcjami autogennego osocza bogatopłytkowego. Kwas hialuronowy pozostaje więc, obok NLPZ, podstawowym środkiem terapeutycznym w leczeniu zachowawczym choroby zwyrodnieniowej stawów. Wiskosuplementacja, czyli podawanie kwasu hialuronowego bezpośrednio do „źródła problemu” – czyli drogą iniekcji dostawowych, jest obecnie standardem w leczeniu zarówno chonodromalacji, doleczania urazowych uszkodzeń chrząstki, jak i choroby zwyrodnieniowej stawów. Mnogość preparatów umożliwia swobodne planowanie terapii i dostosowywanie jej do indywidualnych potrzeb chorego. Dostępne są iniekcje „one shot”- zawierające z reguły hialuronian o wyższym stężeniu i gęstości oraz większej objętości, a także preparaty do podawania w seriach po trzy lub pięć - w zależności od rekomendacji producenta oraz potrzeb chorego. Dostawowa wiskosuplementacja nie tylko poprawia biomechanikę stawu poprzez zmniejszenie sił tarcia w obrębie stawu, ale ma też działanie chondroprotekcyjne oraz przeciwzapalne, co czyni ten typ terapii skutecznym również w przypadkach bardziej zaawansowanych zmian zwyrodnieniowych, gdzie mamy do czynienia z głębokimi ubytkami chrząstki. W świetle obecnych badań terapia z zastosowaniem kwasu hialuronowego wydaje się być „złotym standardem” leczenia zachowawczego zmian zwyrodnieniowych i może być stosowana w szerokich grupach pacjentów.
Kwas hialuronowy, może być stosowany zarówno w zmianach zwyrodnieniowych o charakterze idiopatycznym, jak i pourazowym. Jako integralny składnik chrząstki stawowej, płynu stawowowego oraz tkanki łącznej zapewnia on prawidłową strukturę, właściwości biomechaniczne i fizykochemiczne w obrębie stawów.
Obecnie dostępny jest szeroki wachlarz preparatów kwasu hialuronowego, dedykowanych zarówno do dużych stawów – biodrowy, kolanowy, jak i do małych, np. stawy ręki. Preparaty te są różnego pochodzenia, a sam kwas hialuronowy występuje w odmianach o różnej gęstości i stężeniu, co umożliwia dowolne dostosowanie terapii indywidualnie do każdego chorego.