Żylna choroba zatorowo-zakrzepowa jest jednym z najpoważniejszych powikłań, jakie mogą towarzyszyć rozległym urazom oraz dużym operacjom ortopedycznym, szczególnie w obrębie kończyny dolnej. Obejmuje ona dwie podjednostki chorobowe – ZŻG i ZP. Zgodnie z szacunkami w samych Stanach Zjednoczonych rocznie ok. 900 tys. pacjentów rozwija ŻChZZ, co wiąże się z kilkuset tysiącami hospitalizacji, a ok. 300 tys. przypadków ma śmiertelny skutek, najczęściej w mechanizmie ZP [1–4].
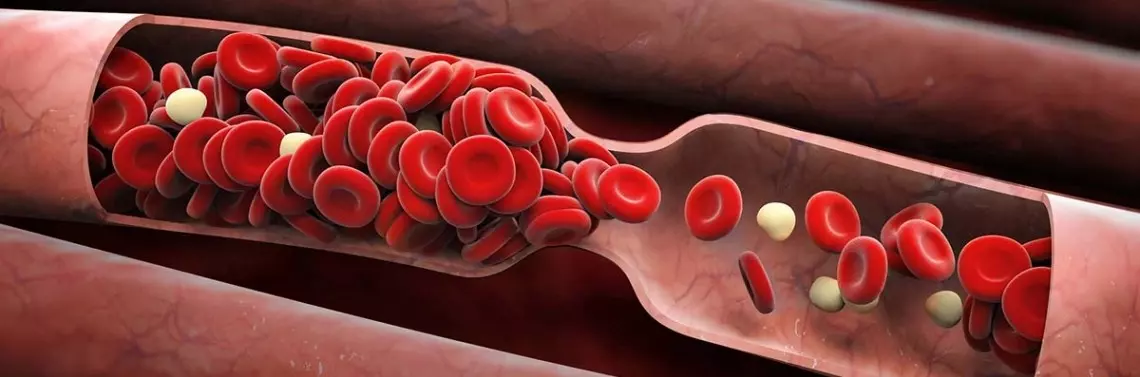
Czynniki ryzyka wystąpienia ŻChZZ dzieli się na zależne od pacjenta i jego stanu klinicznego oraz związane z przeprowadzaną interwencją medyczną, metodami leczenia i profilaktyki. Materiał zakrzepowy najczęściej powstaje w naczyniach żylnych kończyn dolnych. Choroba często przebiega bezobjawowo lub skąpoobjawowo. Wśród najczęściej występujących objawów klinicznych wymienia się: ból i obrzęk łydki, tkliwość i bolesność uciskową, dodatni objaw Homansa, zwiększone ucieplenie kończyny i/lub poszerzenie układu żył powierzchownych [5]. W przypadku ZP objawy, które mogą się pojawić, to duszność i ból w klatce piersiowej. Ponadto może wystąpić uczucie zwiększonej męczliwości, suchy kaszel, krwioplucie, zasłabnięcia, utrata przytomności, a w późniejszym okresie objawy wstrząsu [6]. Około 95% materiału zatorowego skutkującego zatorowością płucną pochodzi z żył kończyn dolnych lub miednicy. Materiał zatorowy może powstać także w innych naczyniach żylnych, np. pachowej czy podobojczykowej, jednak należy to do rzadkości (1–4% przypadków) [4, 7, 13].
Ryzyko poważnych powikłań, takich jak ZP, jest taka sama dla zakrzepów powstających zarówno w kończynach górnych, jak i dolnych.
Szacuje się, że nawet u połowy chorych z ŻChZZ nie udaje się ustalić czynników ryzyka jej wystąpienia i rozpoznaje się postać samoistną [8]. Zgodnie z analizą danych ze Światowego Rejestru Antykoagulantów w aspekcie ŻChZZ (Global Anticoagulant Registry in the FIELD – Venous Thromboembolism), najistotniejszymi czynnikami ryzyka są zabiegi operacyjne (12,5%), hospitalizacja (12%) oraz urazy kończyn dolnych (7,8%) [9]. Głównym mechanizmem śmierci pacjentów z ostrą ZP jest niewydolność prawokomorowa serca [4]. U ok. 1/3 chorych z ZP wcześniej pojawiają się objawy ZŻG [5]. Do wystąpienia ŻChZZ predysponują wszystkie stany zaburzające hemostazę triady Virchowa: zwolnienie przepływu krwi (w wyniku ucisku lub unieruchomienia), uszkodzenie ściany naczynia (urazy) lub stany zwiększające krzepliwość krwi (przewaga czynników prozakrzepowych) [5]. Chirurgia ortopedyczna, szczególnie dużych stawów, wpływa na zaburzenia w obrębie wszystkich trzech składowych triady Virchowa [6]. Zgodnie z danymi w okresie miesiąca od dokonania rozpoznania ŻChZZ umiera 6% pacjentów z ZŻG i 12% z rozpoznaną ZP [10]. Należy podkreślić, że nawet wśród pacjentów bez czynników ryzyka, chorób współistniejących i z prawidłową profilaktyką przeciwzakrzepową chory jest narażony na wystąpienie ZP [11].
Wczesne rozpoznanie ZŻG i ZP jest kluczowe dla poprawy rokowania pacjentów, zmniejszenia odsetka śmiertelności oraz skrócenia czasu hospitalizacji [12]. Czynniki ryzyka wystąpienia ŻChZZ w chirurgii ortopedycznej i traumatologii według De Anderson i Baksaca zostały przedstawione w tabeli 1 [2].
REKLAMA
Żylna choroba zakrzepowo-zatorowa w traumatologii
U większości pacjentów po rozległych urazach obserwuje się zwiększoną aktywność czynników, kaskady krzepnięcia i zmniejszenie aktywności procesu fibrynolizy [13]. W części przypadków może być obecne istotne uszkodzenie naczyń krwionośnych. Należy podkreślić częstą konieczność długotrwałego unieruchomienia pacjentów z tej kohorty. W związku z zaburzeniem każdej ze składowych triady Virchowa pacjenci po urazach są grupą szczególnie narażoną na wystąpienie różnych koagulopatii, których końcowym efektem może być ZŻG oraz ZP [14]. Zgodnie z danymi częstość występowania ŻChZZ u chorych po urazach szacuje się w granicach 7–58% [14]. Odsetek powikłań jest związany z zastosowaniem profilaktyki przeciwzakrzepowej. Niektóre źródła sugerują, że odsetek ZŻG u pacjentów po rozległych urazach bez profilaktyki może wynosić 50%, a w przypadku zastosowania profilaktyki – 44% [13, 15, 16].
U pacjentów po urazach wielonarządowych, którzy przeżyli ponad 24 godziny od wypadku, uznaje się, że ZP stanowi trzecią co do kolejności przyczynę zgonów [14, 17]. Szacuje się, że u 25% pacjentów po rozległych urazach w momencie przyjęcia do szpitala obecne są zmiany koagulopatyczne, a śmiertelność w tej kohorcie jest niemal pięć razy wyższa niż u chorych bez wyjściowych koagulopatii [18].
Zgodnie z wynikami badania Najari i wsp. [1] częstość zgonów spowodowana ZP w kohorcie liczącej 10 800 wynosiła 0,85%. Większość doznała urazów kończyn dolnych (45%), głowy (36%), rdzenia kręgowego (10%) oraz kończyny górnej (1%) w następstwie wypadków samochodowych (64%), upadków (18%) oraz napaści. Podobne badanie Ho i wsp. [19] wykazało odsetek zgonów spowodowanych ZP po urazach na poziomie 1,6%, a badanie Echeverria i wsp. [20] – 2,75%.
Część autorów sugeruje, że w grupie pacjentów umiarkowanego i wysokiego ryzyka rozwinięcia się ŻChZZ wskazane może być przesiewowe badanie USG kończyn dolnych (lower extremity duplex ultrasound screening – LEDUS). Martin i wsp. [13] określali grupy ryzyka na podstawie skali oceny ryzyka (risk assessment profile – RAP). U pacjentów z wynikami RAP na poziomie 7–9 odsetek powikłań wynosił 15,4% w porównaniu do 6,1% u chorych z wynikiem 5–6. W związku z uzyskanymi wynikami autorzy sugerują, że USG pod kątem zmian zakrzepowych może być wskazane u chorych po ciężkich urazach, którzy uzyskali 7 lub więcej punktów w skali RAP. Inne badania wykazują predykcyjne znaczenie D-dimerów w określaniu ryzyka wystąpienia powikłań zatorowo-zakrzepowych [12]. Jako że w przypadku pacjentów po urazach poziom D-dimerów może być podwyższony wyjściowo, Iyamata i wsp. [12] sugerują oznaczenie przez trzy dni z rzędu u chorych hospitalizowanych powyżej pięciu dni. W przypadku wartości rosnących, szczególnie przewyższających 15 mikrogramów/mL, można poszerzyć diagnostykę o tomografię komputerową ze wzmocnieniem kontrastowym. W swojej pracy na grupie 455 pacjentów po zastosowaniu takiego protokołu określili oni skuteczność pozytywnej wartości predykcyjnej w rozpoznawaniu bezobjawowej zatorowości żylnej na poziomie 46,6%.
Żylna choroba zakrzepowo-zatorowa a zabiegi ortopedyczne
Relatywnie największe ryzyko wystąpienia ŻChZZ jest związane z dużymi operacjami miednicy i kończyny dolnej. Zgodnie z danymi odsetek ZŻG podudzia u pacjentów poddanych aloplastyce stawu biodrowego lub kolanowego może sięgać 20–40% [21]. Zgodnie z niektórymi badaniami ŻChZZ jest rozpoznawana u 0,5% pacjentów kwalifikowanych do całkowitej lub częściowej aloplastyki stawu biodrowego, a w trzymiesięcznym okresie po wypisie – 2–5% pacjentów [22, 23]. W przypadku zabiegów rewizyjnych ryzyko nieco wzrasta [24]. Szczególnie w przypadku operacji stawu kolanowego podkreśla się zaburzenia składowych klasycznej triady Virchowa poprzez zmniejszenie przepływu krwi, zaburzenia krzepnięcia, niedokrwienie, uszkodzenie naczyń krwionośnych, używanie opaski uciskowej oraz długotrwałe unieruchomienie kolana w nadmiernym zgięciu [25]. Shin i wsp. [25] badali korelację relatywnej objętości mięśni z ryzykiem wystąpienia ZŻG po aloplastyce stawu kolanowego. Zgodnie z wynikami niska masa mięśnia obszernego bocznego może być związana z podwyższonym ryzykiem wystąpienia zakrzepicy w okresie pooperacyjnym. Jedne z danych sugerują, że w przypadku braku profilaktyki przeciwzakrzepowej przy planowych operacjach aloplastyki
stawu kolanowego i biodrowego aż u 50% pacjentów rozwija się ŻChZZ, w tym u 5% objawowa [26].
W przypadku operacji miednicy oraz panewki stawu biodrowego Dweyer i wsp. [27] określili ryzyko wystąpienia ŻChZZ w okresie 90 dni od wypisu ze szpitala na poziomie 0,83%. W większości przypadków pod postacią ZŻG, następnie ZP, a u 0,12% odnotowano ZŻG i ZP.
W niektórych kohortach pacjentów, tj. u chorych z hemofilią, rutynowa profilaktyka przeciwzakrzepowa w formie leków nie jest stosowana okołooperacyjnie i pooperacyjnie. Wyniki niedawno opublikowanego badania autorstwa Peng i wsp. [28] na kohorcie 98 pacjentów z hemofilią poddanych aloplastyce stawów biodrowych i/lub kolanowych również zachęcają w tej grupie chorych do stosowania profilaktyki mechanicznej, a nie w formie leków. Autorzy odnotowali odsetek ZŻG na poziomie 1,02%.
Zgodnie z wynikami kohortowego badania na podstawie Szwedzkiego Rejestru Zabiegów na Więzadłach Stawu Kolanowego (Swedish Knee Ligament Register) z lat 2006–2013 ŻChZZ dotyczyła 0,4% pacjentów poddanych pierwotnym i rewizyjnym rekonstrukcjom więzadła krzyżowego przedniego [29]. W badaniu 94% przypadków stanowiła ZŻG, pozostałe 6% – ZP.
Istnieją ograniczone doniesienia dotyczące wystąpienia ZŻG po operacjach na kończynie górnej. W zależności od różnych źródeł jest ono oceniane na 0,02–13% [30, 31]. Takahashi i wsp. [32] odnotowali 5,7% powikłań zakrzepowych w grupie 175 pacjentów poddanych planowym artroskopiom stawu ramiennego. Wśród procedur znajdowała się artroskopowa rekonstrukcja stożka rotatorów, operacje nawrotowych zwichnięć stawu ramiennego, uszkodzeń Bankarta oraz patch graft procedure. Scott i wsp. [33] opisali przypadek pacjenta poddanego zabiegowi oczyszczania stawu ramiennego powikłanego zakrzepicą żyły ramiennej i ZP. Rockwood i wsp. [34] przedstawili przypadki dwóch pacjentów z ZP po planowych operacjach stawu ramiennego. Li i wsp. [7] opisali przypadek pacjentki po złamaniu bliższego końca kości ramiennej leczonego stabilizacją z wykorzystaniem płyty, u której wystąpiła zakrzepica żyły podobojczykowej oraz ZP ze skutkiem śmiertelnym. Zasadniczo ryzyko ŻChZZ powikłanej zatorem płucnym jest wyższe dla zabiegów aloplastyki stawów ramiennych oraz po złamaniach niż dla planowych procedur artroskopowych [31]. W przypadku pacjentów o wysokim ryzyku powikłań zakrzepowo-zatorowych należy zastanowić się nad zastosowaniem profilaktyki przeciwzakrzepowej. U każdego chorego warto rozważyć profilaktykę z wykorzystaniem mechanicznych metod kompresyjnych [31]. W obowiązujących obecnie w Polsce wytycznych [6] u pacjentów z izolowanymi urazami kończyn górnych nie zaleca się rutynowej profilaktyki przeciwzakrzepowej. Profilaktykę ŻChZZ w tej grupie chorych należy rozważyć u pacjentów z następującymi czynnikami ryzyka: koagulopatie, choroby nowotworowe, obecność centralnych dostępów żylnych, przebyta ŻChZZ oraz u pacjentów w podeszłym wieku poddawanym aloplastyce stawu ramiennego po indywidualnej ocenie czynników ryzyka. W tych sytuacjach zalecana jest profilaktyka przez 5–7 dni z zastosowaniem heparyn drobnocząsteczkowych.
Żylna choroba zakrzepowo-zatorowa – zarys diagnostyki i strategii leczenia
Uproszczony algorytm kliniczny rozpoznawania ZŻG [5]:
- kliniczne podejrzenie zakrzepicy – należy wykonać doppler USG naczyń żylnych,
- w przypadku dodatniego wyniku badania – potwierdzenie zakrzepicy,
- w przypadku negatywnego wyniku badania i z równoczesnym silnym podejrzeniem zakrzepicy na podstawie objawów klinicznych zaleca się oznaczenie poziomu D-dimerów,
- D-dimery negatywne – wykluczenie zakrzepicy,
- D-dimery pozytywne (należy pamiętać, że podwyższony poziom D-dimerów może być wynikiem samych zabiegów operacyjnych lub urazów) – powtórzyć badanie doppler USG naczyń żylnych za 2–3 dni lub wykonać flebografię.
| Czynniki ryzyka o znaczeniu | ||
| wysokim | średnim | niskim |
|
Złamanie bliższego końca kości Endoprotezoplastyka stawu Duże zabiegi Uszkodzenia rdzenia |
Chemioterapia Niewydolność serca |
Pobyt w łóżku powyżej 3 dni Zaawansowany wiek Chirurgia artroskopowa Nadwaga Żylaki |
Uproszczony algorytm kliniczny rozpoznawania ZP [5]:
- podejrzenie ZP – ocena w skali Wellsa,
- jeśli prawdopodobieństwo jest niskie (< 4 pkt):
Czy pacjent spełnia kryteria wykluczenia ZP?
Tak —> ZP wykluczona
Nie —> oznaczenie D-dimerów (jeśli negatywne – ZP wykluczona, jeśli pozytywne diagnostykę należy rozszerzyć o badanie angiograficzne tomografii komputerowej), - jeśli prawdopodobieństwo jest umiarkowane (4–5 pkt): badanie angiograficzne tomografii komputerowej – wynik pozytywny potwierdza, negatywny – należy oznaczyć D-dimery,
- jeśli prawdopodobieństwo jest wysokie (> 6 pkt): postępowanie jest analogiczne jak w punkcie 3, przy czym należy niezwłocznie od podejrzenia ZP rozpocząć leczenie antykoagulacyjne.
Zarys leczenia ZŻG:
- Leczenie przeciwkrzepliwe ma znaczenie podstawowe.
- Leczenie postaci bezobjawowej i objawowej jest takie samo.
- W przypadku niewielkiego nasilenia objawów i świeżo rozpoznanej ZŻG terapię można prowadzić w warunkach domowych.
- Należy zalecać wczesne, pełne uruchomienie (poza dniem rozpoznania i rozpoczęcia leczenia heparyną tego dnia zalecane jest leżenie w łóżku z uniesioną kończyną dolną).
- Zaleca się leczenie stopniowanym uciskiem.
- U pacjentów, którzy mają przeciwwskazania do długotrwałego leczenia przeciwkrzepliwego, należy rozważyć wszczepienie filtru do żyły głównej dolnej.
- W wybranych przypadkach należy rozważyć celowane leczenie trombolityczne.
- W przypadkach utrzymującego się obrzęku u pacjentów obciążonych czynnikami ryzyka ŻChZZ po zakończeniu standardowej profilaktyki ŻChZZ warto rozważyć w okresie rehabilitacji dodatkowe leczenie farmakologiczne. W takich przypadkach warto w tym okresie zastosować leczenie sulodeksydem, który jest lekiem zaliczanym do grupy pochodnych heparyn. Sulodeksyd wykazuje działanie przeciwzakrzepowe związanie głównie z hamowaniem czynnika Xa, które wzmacniane jest hamowaniem adhezji płytek krwi oraz aktywacją układu fibrynolitycznego. Sulodeksyd zmniejsza ryzyko wystąpienia zakrzepicy u chorych wysokiego ryzyka poprzez poprawę reologicznych właściwości krwi przez zmniejszenie stężenia fibrynogenu. Zastosowanie Sulodeksydu przyczynia się również do zmniejszenia obrzęku kończyn dolnych, który może wtórnie być powodem wystąpienia zakrzepicy. Terapia z użyciem sulodeksydu powinna mieć zastosowanie u pacjentów, którzy zakończyli standardowe leczenie przeciwzakrzepowe (od 3 do 12 miesięcy) z powodu zakrzepicy żył głębokich lub zatorowości płucnej, a także u chorych z czynnikami ryzyka po przeprowadzonej dużej operacji ortopedycznej. W naszej praktyce często spotykamy się z występowaniem niespecyficznych obrzęków kończyn dolnych, które po przeprowadzonych dają uczucie dyskomfortu, utrudniając pacjentom powrót do pełnej aktywności.
Podsumowanie
Żylna choroba zakrzepowo-zatorowa jest jednym z najpoważniejszych powikłań mogących towarzyszyć rozległym urazom oraz dużym procedurom ortopedycznym. Podczas leczenia kluczowa jest czujność lekarza oraz znajomość czynników ryzyka związanych zarówno z procesami leczniczymi, jak i z pacjentem w celu wdrożenia odpowiedniego postępowania profilaktycznego lub leczniczego. Działania takie pozwalają na zredukowanie liczby ciężkich powikłań ŻChZZ, ze zgonem włącznie.
PIŚMIENNICTWO
- Gajewski RP. Interna Szczeklika. Podręcznik chorób wewnętrznych. Kraków: Medycyna Praktyczna; 2013.
- Chmielewski D, Gorecki A, Kusz D, Maldyk P, Marczynski W, Tomkowski W. [Principles of prevention of venous thromboembolism in orthopedics and traumatology (updated on 02/18/2014)]. Ortop Traumatol Rehabil. 2014;16(2):227-39.
- Heit JA, Silverstein MD, Mohr DN, Petterson TM, O’Fallon WM, Melton LJ, 3rd. Predictors of survival after deep vein thrombosis and pulmonary embolism: a population-based, cohort study. Arch Intern Med. 1999;159(5):445-53.
- Iyama K, Inokuma T, Sato S, Yamano S, Tajima G, Hirao T, et al. Novel screening criteria for post-traumatic venous thromboembolism by using D-dimer. Acute Med Surg. 2019;6(1):40-8.
- Martin GE, Pugh A, Williams SG, Hanseman D, Nomellini V, Makley AT, et al. Lower Extremity Duplex Ultrasound Screening Protocol for Moderate- and High-Risk Trauma Patients. J Surg Res. 2019;235:280-7.
- Najari F, Mostafazadeh B, Akbari A, Baradaran Kaya I, Najari D. Characteristics of Mortalities related to Pulmonary Embolism following Multiple Trauma; a Brief Report. Emerg (Tehran). 2018;6(1):e48.
- Brohi K, Singh J, Heron M, Coats T. Acute traumatic coagulopathy. J Trauma. 2003;54(6):1127-30.
- Ho KM, Burrell M, Rao S, Baker R. Incidence and risk factors for fatal pulmonary embolism after major trauma: a nested cohort study. Br J Anaesth. 2010;105(5):596-602.
- Echeverria RF, Baitello AL, Pereira de Godoy JM, Espada PC, Morioka RY. Prevalence of death due to pulmonary embolism after trauma. Lung India. 2010;27(2):72-4.
- Group JCSJW. Guidelines for the diagnosis, treatment and prevention of pulmonary thromboembolism and deep vein thrombosis (JCS 2009). Circ J. 2011;75(5):1258-81.
- Shin JM, Hong SJ, Choi KH, Shin SI, Lee DK, Lee SS, et al. Low relative muscle volume: Correlation with prevalence of venous thromboembolism following total knee arthroplasty. PLoS One. 2019;14(3):e0210800.
- Dwyer EP, Moed BR. Venous thromboembolism after hospital discharge in pelvic and acetabular fracture patients treated operatively. J Orthop Surg (Hong Kong). 2019;27(1):2309499019832815.
- Peng HM, Wang LC, Zhai JL, Jiang C, Weng XS, Feng B, et al. Incidence of Symptomatic Venous Thromboembolism in Patients with Hemophilia Undergoing Hip and Knee Joint Replacement without Chemoprophylaxis: A Retrospective Study. Orthop Surg. 2019.
- Kraus Schmitz J, Lindgren V, Janarv PM, Forssblad M, Stalman A. Deep venous thrombosis and pulmonary embolism after anterior cruciate ligament reconstruction: incidence, outcome, and risk factors. Bone Joint J. 2019;101-B(1):34-40.
- Scott DL. Pulmonary embolism after elective glenohumeral joint debridement. Orthopedics. 2001;24(5):495-7.
- Rockwood CA, Jr., Wirth MA, Blair S. Warning: pulmonary embolism can occur after elective shoulder surgery-report of two cases and survey of the members of the American Shoulder and Elbow Surgeons. J Shoulder Elbow Surg. 2003;12(6):628-30.
- Aibinder WR, Sanchez-Sotelo J. Venous Thromboembolism Prophylaxis in Shoulder Surgery. Orthop Clin North Am. 2018;49(2):257-63.