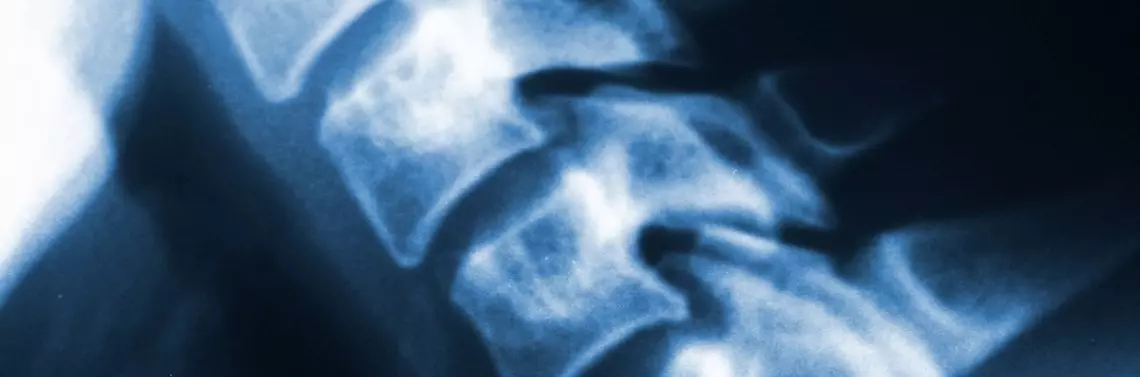
Kręgosłup jest jedną z najczęstszych lokalizacji złamań struktur układu ruchu w przebiegu osteoporozy. Złamania kręgów występują u blisko 20% osób w wieku starszym i odpowiadają w znacznym stopniu za pogorszenie jakości życia [1]. Poza osteoporozą do grupy czynników zwiększających ryzyko wystąpienia złamania kompresyjnego kręgosłupa należą także choroby niekorzystnie wpływające na tkankę kostną, np. reumatoidalne zapalenie stawów (RZS) czy cukrzyca [2]. Reumatoidalne zapalenie stawów jest przewlekłą chorobą zapalną o podłożu autoimmunologicznym, występującą u ok. 1% populacji krajów uprzemysłowionych [3]. Choroba jest stwierdzana 2–3 razy częściej u kobiet w porównaniu z mężczyznami [3].
Cechuje się symetrycznym zapaleniem stawów oraz objawami wynikającymi z zajęcia procesem chorobowym narządów wewnętrznych. Wśród struktur układu ruchu, które szczególnie często są uszkadzane w przebiegu RZS, jest kręgosłup. W RZS dochodzi do ubytku masy kostnej oraz miejscowych zmian o charakterze erozji kości [4]. Procesy erozyjne w największym stopniu lokalizują się w warstwie podchrzęstnej i warstwie korowej kości [4]. Zjawiska te poza stawami występują także w osiowej części układu ruchu, wpływając na jego wytrzymałość. Struktury kostne kręgosłupa są szczególnie narażone na szybki rozwój tych zmian w przypadku braku odpowiedniego leczenia choroby podstawowej [5].
W wyniku opisanych wyżej zmian zagrożenie złamaniem kręgu u pacjentów z RZS zwiększa się dwukrotnie w porównaniu z grupą w podobnym wieku [6]. Złamania kompresyjne kręgosłupa w grupie pacjentów z RZS stanowią poważny problem kliniczny. Decydują o takiej opinii duża częstość występowania złamań w tej grupie chorych, brak klarownych zasad diagnozowania pacjentów z podejrzeniem złamania kompresyjnego kręgu oraz nagminne odstępowanie w codziennej praktyce klinicznej od przyjętych zasad leczenia złamań kompresyjnych kręgosłupa.
REKLAMA
Diagnozowanie złamań kompresyjnych kręgów
W grupie pacjentów z osteoporozą złamanie jednego kręgu zwiększa prawdopodobieństwo występowania złamań w innych częściach kręgosłupa 5–12, krotnie [7].
Badania podmiotowe i przedmiotowe umożliwiają rozpoznanie jednego na cztery złamania kompresyjne rozwijające się w przebiegu osteoporozy [8]. Dodatkowo wykonanie tylko badania radiologicznego (RTG) w 34–50% przypadków nie daje możliwości rozpoznania złamania kompresyjnego kręgów [9]. Fakt ten wymusza zastosowanie badań diagnostycznych o zwiększonej czułości w grupie pacjentów z osteoporozą i podejrzeniem złamania kręgu. Do badań tych należy w pierwszej kolejności MRI i jako badanie drugiego rzutu tomografia komputerowa (computed tomography – CT). Pozostałe metody diagnostyczne, takie jak scyntygrafia czy pozytonowa tomografia emisyjna sprzężona z tomografią komputerową (positron emission tomography/computed tomography – PET/CT), są rzadko wykonywane. W procesie diagnostycznym złamań, których etiologia nie jest jednoznaczna, wykorzystywane jest także badanie histopatologiczne materiału biopsyjnego uzyskanego np. w trakcie wykonywania zabiegu cementoplastyki.
Leczenie zachowawcze i chirurgiczne złamań kompresyjnych
Wynik badania neurologicznego ma podstawowe znaczenie podczas kwalifikowania pacjentów do leczenia zachowawczego lub chirurgicznego. Objawy ubytkowe neurologiczne wskazują z zasady na potrzebę leczenia chirurgicznego. Kolejną wskazówką pozwalającą prawidłowo wybrać rodzaj leczenia jest ocena stopnia niestabilności, jakie wywołuje złamanie kręgów i uraz tkanek otaczających kręgosłup. Złamanie z przemieszczeniem sąsiadujących odłamów kręgów, urazy zgięciowo-dystrakcyjne i złamania wybuchowe z towarzyszącym znacznym przemieszczeniem odłamów do światła kanału kręgowego wymagają leczenia chirurgicznego. Leczenie zachowawcze, w tym ortezy, mogą być stosowane w grupie pacjentów bez objawów neurologicznych i ze złamaniami, które nie powodują niestabilności kręgosłupa. Duża część złamań z klinowatą zmianą kształtu trzonu kręgu może być leczona przez 2–3 miesiące z zastosowaniem ortez. W tych przypadkach głównym celem zastosowania ortezy jest zapobieganie obciążeniom przedniej części trzonów rozwijającym się podczas ruchu zgięcia do przodu. Gdy złamanie klinowe kręgu przebiega z 50-procentowym zmniejszeniem wysokości trzonu i/lub złamanie miejscowo powoduje istotną zmianę osi w płaszczyźnie strzałkowej (kifotyzacja większa niż 30 stopni), i/lub złamanie obejmuje trzy sąsiadujące ze sobą kręgi, powinno być rozpatrzone leczenie operacyjne [10]. Ważna dla praktyka jest także informacja, że nie wszystkie złamania, którym towarzyszy przemieszczenie odłamów do kanału kręgowego, wymagają leczenia chirurgicznego. Złamania bez klinicznych objawów uszkodzenia struktur nerwowych i zwężenie kanału kręgowego do 50% także mogą być leczone zachowawczo [10].

Leczenie nieoperacyjne jest zarezerwowane dla osób niespełniających kryteria leczenia zabiegowego oraz osób, które nie mogą być leczone chirurgicznie w związku z chorobami dodatkowymi. Podstawowym jego elementem jest odciążenie kręgosłupa w okresie ostrym. W praktyce jest to zalecenie zmniejszenia aktywności fizycznej do minimum oraz stosowanie ortez. Zalecenie ograniczające aktywność fizyczną powinno zawężać się do jak najkrótszego okresu po złamaniu w związku z ryzykiem wystąpienia potencjalnych powikłań związanych z unieruchomieniem pacjenta. Ortezy stosowane w populacji pacjentów ze złamaniami kompresyjnymi w przebiegu chorób pogarszających jakość kości nie mają jednoznacznie pozytywnych opinii [11]. Powodem tego jest brak wpływu ortez na stopień narastania patologicznych krzywizn, wynikający ze złamania kręgosłupa. Fizykoterapia może wspomagać w okresie ostrym zwalczanie bólu towarzyszącego złamaniu. Podstawowym jednak sposobem leczenia bólu jest farmakoterapia stosowana zgodnie z zasadami opisanymi w drabinie analgetycznej Światowej Organizacji Zdrowia oraz leczenie farmakologiczne osteoporozy.
Gdy ból ustępuje, pacjenci powinni mieć zleconą kinezyterapię. W przypadku osób, u których złamanie spowodowało zaburzenie balansu strzałkowego, istotne znaczenie ma stosowanie sprzętu rehabilitacyjnego odciążającego kręgosłup, np. balkoników, podpórek czy kul. Ma to także olbrzymie znaczenie w profilaktyce upadków. Bardzo ważne jest uświadomienie sobie, że żaden sposób leczenia zachowawczego nie zatrzyma progresji zaburzeń balansu strzałkowego rozwijającego się w wyniku złamania [12]. Duże znaczenie w podejmowaniu decyzji o wyborze sposobu leczenia ma także czas, jaki upłynął od pojawienia się pierwszych objawów złamania. Ból utrzymujący się powyżej czterech tygodni, mimo pełnego leczenia przeciwbólowego i stosowania ortezy, powinien być czynnikiem wymuszającym ocenę negatywną sposobów dotychczasowego leczenia i wybór innych metod stosowanych w leczeniu złamań kompresyjnych trzonów.
Wertebroplastyka – najczęstsze wskazanie do wykonania cementoplastyk stanowi ból, którego przyczyną jest niekwalifikujące się do zaopatrzenia innymi metodami chirurgicznymi złamanie kompresyjne trzonu potwierdzone w badaniu obrazowym i niepoddające się leczeniu zachowawczym. Wskazaniem do wykonania zabiegu są także niezrastające się złamania trzonów, wywołujące ból oraz złamania w przebiegu jałowej martwicy trzonów. Cementoplastyki wykonywane są także u osób ze zmianami osteolitycznymi w przebiegu choroby nowotworowej.
Kyfoplastyka – kwalifikacją do tego typu cementoplastyki, której zadaniem jest zmniejszenie deformacji trzonu kręgu, objęte są złamania o charakterze wgnieceń blaszek granicznych trzonów kręgów, złamania z obniżeniem przedniej części trzonu (złamania klinowe) oraz z symetrycznym obniżeniem całej jego wysokości, a także złamania wybuchowe częściowe, z zachowaną ciągłością tylnej ściany trzonu (zdj. 1). Do wykonania tego typu zabiegu kwalifikują się także patologie nowotworowe przebiegające z miejscową osteolizą.
Sakroplastyka – złamaniu w przebiegu osteoporozy może także ulegać kość krzyżowa. Złamania te są jedno- lub obustronne. Leczenie stosowane u większości pacjentów ze złamaniami kości krzyżowej ma charakter zachowawczy. Efekty leczenia zachowaw czego u dużego odsetka pacjentów są jednak niezadowalające. Na negatywną ocenę rezultatów leczenia zachowawczego tych złamań wpływa przedłużające się ograniczenie aktywności ruchowej, które jest wywołane bólem. Rezultaty leczenia operacyjnego wykonywanego w znieczuleniu ogólnym i polegającego na ustabilizowaniu odłamów kostnych za pomocą materiałów zespalających nie zawsze są dobrze oceniane przez pacjentów. Wynika to z powikłań towarzyszących znieczuleniu ogólnemu i skutków działania implantów na osłabioną strukturę kości u pacjentów z osteoporozą. Alternatywą dla pacjentów ze złamaniami kości krzyżowej towarzyszącymi osteoporozie są zabiegi sakroplastyki. Po raz pierwszy zabieg ten opisał Garant w 2002 r. [13] Od tego czasu metoda jest stosowana w przypadku złamań, którym towarzyszy przewlekający się ból niereagujący na zachowawcze metody leczenia. Pewnej kwalifikacji do zabiegów sakroplastyki podlegają złamania w strefie pierwszej według klasyfikacji Denisa. Kwalifikacja do zabiegu sakroplastyki w przypadku innych rodzajów złamań musi być rozpatrywana indywidualnie. W większości przypadków złamania kości krzyżowej w przebiegu osteoporozy kwalifikują się do grupy, w której można wykonać sakroplastykę (zdj. 2).

Implanty dotrzonowe z cementem kostnym – wskazania do wykonywania tego typu zabiegów stale się rozszerzają (zdj. 3). Obecnie do zabiegów kwalifikowani są pacjenci z obniżeniem wysokości trzonów o co najmniej 15–35% i miejscowym patologicznym zagięciem kifotycznym powyżej 15 stopni. Do zabiegu kwalifikowani są także pacjenci, u których w wyniku złamania tylna ściana trzonu uległa zmniejszeniu o nie więcej niż 25%, oraz pacjenci z wytworzonymi stawami rzekomymi trzonów. Zabiegi te nie powinny być wykonywane w złamaniach, które uległy samoistnemu wygojeniu.
Stabilizacja wewnętrzna kręgosłupa – operacje tego typu wykonuje się w przypadkach występowania objawów neurologicznych wymagających odbarczenia kanału kręgowego, w przypadku złamań niestabilnych opisywanych powyżej oraz w przypadku takich rodzajów złamań, które uniemożliwiają wykonanie zabiegu cementoplastyki (zdj. 4).


Podsumowanie
W przebiegu RZS dochodzi do zaniku masy kostnej i erozji warstwy korowej i podchrzęstnej kręgów. W wyniku tego zaburzona zostaje architektura kości i wytrzymałość mechaniczna trzonu kręgu. Podstawową przyczyną tego zjawiska jest zaburzenie równowagi czynnościowej między osteoklastami i osteoblastami [14].
Drugim ważnym czynnikiem w powstawaniu złamań kręgosłupa w grupie pacjentów z RZS jest proces zapalny toczący się w tkankach miękkich sąsiadujących ze strukturami kostnymi. Cytokiny prozapalne wpływają niekorzystnie także na równowagę aktywności między osteoklastami i osteoblastami [15]. Dodatkowo leczenie glikokortykosteroidami podnosi ryzyko wystąpienia osteopenii i osteoporozy u tych chorych [16]. W grupie pacjentów z RZS proces diagnozowania złamań powinien być skrócony do minimum. W praktyce oznacza to sięganie w pierwszej kolejności do badań obrazowych (tzn. MRI i w drugiej kolejności CT) w przypadkach pacjentów z podejrzeniem złamania kompresyjnego. Wybór leczenia powinien opierać się ściśle na opisanych kryteriach ustalonych na podstawie potwierdzonych statystycznie danych medycznych.
Piśmiennictwo
- Schousboe J.T. Epidemiology of vertebral fractures. J Clin Densitom 2016; 19: 8–22.
- Wang J., You W., Jing Z. i wsp. Increased risk of vertebral fracture in patients with diabetes: a meta-analysis of cohort studies. Int Orthop 2016; 40: 1299–1307.
- Gibofsky A. Overview of epidemiology, pathophysiology, and diagnosis of rheumatoid arthritis. Am J Manag Care 2012; 18 (13 Suppl): S295–S302.
- Deal C. Bone loss in rheumatoid arthritis: systemic, periarticular, and focal. Curr Rheumatol Rep 2012; 14: 231–237.
- Schett G., Gravallese E. Bone erosion in rheumatoid arthritis: mechanisms, diagnosis and treatment. Nat Rev Rheumatol 2012; 8: 656–664.
- Xue A.L., Wu S.Y., Jiang L. i wsp. Bone fracture risk in patients with rheumatoid arthritis: A meta-analysis. Medicine (Baltimore) 2017; 96 (36): e6983.
- Melton L.J. 3rd, Atkinson E.J., Cooper C. i wsp. Vertebral fractures predict subsequent fractures. Osteoporos Int 1999; 10 (3): 214–221.
- Fink H.A., Milavetz D.L., Palermo L. i wsp. What proportion of incident radiographic vertebral deformities is clinically diagnosed and vice versa? J Bone Miner Res 2005; 20 (7): 1216–1222.
- Delmas P.D., van de Langerijt L., Watts N.B. i wsp.; IMPACT Study Group. Under diagnosis of vertebral fractures is a worldwide problem: the IMPACT study. J Bone Miner Res 2005; 20 (4): 557–563.
- Rea G.L., Zerick W.R. The treatment of thoracolumbar fractures: one point of view. J Spinal Disord 1995; 8: 368–382.
- Esses S.I., McGuire R., Jenkins J. i wsp. American Academy of Orthopaedic Surgeons clinical practice guideline on: the treatment of osteoporotic spinal compression fractures. J Bone Joint Surg Am 2011; 93: 1934–1936.
- Iwata A., Kanayama M., Oha F. i wsp. Effect of teriparatide (rh-PTH 1-34) versus bisphosphonate on the healing of osteoporotic vertebral compression fracture: a retrospective comparative study. BMC Musculoskelet Disord 2017; 18 (1): 148.
- Garant M. Sacroplasty: a new treatment for sacral insufficiency fracture. J Vasc Interv Radiol 2002; 13: 1265–1267.
- Haynes D.R., Crotti T.N., Loric M. i wsp. Osteoprotegerin and receptor activator of nuclear factor kappaB ligand (RANKL) regulate osteoclast formation by cells in the human rheumatoid arthritic joint. Rheumatology (Oxford) 2001; 40: 623–630.
- Jung S.M., Kim K.W., Yang C.W. i wsp. Cytokine-mediated bone destruction in rheumatoid arthritis. J Immunol Res 2014; 2014: 263625.
- Vis M., Guler-Yuksel M., Lems W.F. Can bone loss in rheumatoid arthritis be prevented? Osteoporos Int 2013; 24: 2541–2553.