W1952 roku Herman Kabat opracował system ćwiczeń PNF (ang. proprioceptive neuromus-cular facilitation) dedykowanych głównie dla usprawniania chorych po udarach [1], a w 1965 roku Vaclav Vojta rozwinął metodę kinezyterapii u niemowląt, opartą na mechanizmach odruchowej lokomocji [2, 3], w obu przypadkach pod wyraźnym wpływem wyników badań neurofizjologicznych i neuroanatomicznych sir Charlesa Sherringtona [3]. Neurofizjologia kliniczna była również wielokrotnie wykorzystywana do oceny skuteczności elektroterapii funkcjonalnej mięśni niedowładnych w terapii chorych po udarach [4, 5], ale w programowaniu parametrów aplikowanych bodźców elektrycznych zwykle nie uwzględniano oceny stanu funkcjonalnego układów mięśniowego i nerwowego przed podjęciem leczenia. Obecnie leczenie chorych po udarach niedokrwiennych oparte jest na założeniu ponownego wyuczenia funkcji ruchowych odnoszących się do zjawiska neuroplastyczności na poziomie zarówno czynności ośrodków rdzenia, jak i ośrodków nadrdzeniowych [6, 7].
Najpowszechniej stosowaną formą kinezyterapii są zabiegi PNF, często uzupełniane funkcjonalną stymulacją mięśni działających antagonistycznie na poziomie stawu nadgarstka i skokowego [8], gdzie objawy spastyczności i dysfunkcji jednostek ruchowych manifestują się najbardziej. Lisiński i wsp. [8], podobnie jak Kraft i wsp. [9], wykorzystywali w leczeniu chorych po udarach zabiegi PNF skojarzone z funkcjonalną stymulacją elektryczną mięśni i wykazali znaczącą poprawę funkcji mięśni niedowładnych kończyn górnych i dolnych. Jednakże badania w tym zakresie wykonywane były w odniesieniu do obserwacji krótkoterminowej, najdłużej po 20 dniach leczenia.
Na podstawie przeglądu literatury można stwierdzić, że podstawowym problemem związanym ze skutecznością zabiegów elektrostymulacji mięśni lub nerwów jest wykorzystanie algorytmów bodźców elektrycznych standardowo dostarczanych wraz ze sprzętem do elektroterapii przez producentów. Spersonalizowanie algorytmów stymulacyjnych pozostawia nadal wiele do życzenia, jeżeli chodzi o indywidualizację dla potrzeb usprawnianego chorego, co stanowi jedno z wyzwań omawianej w pracy terapii.
Celem artykułu jest przedstawienie metodologii i wstępnych wyników diagnostyki i leczenia z wykorzystaniem zmodyfikowanej funkcjonalnej stymulacji nerwowo-mięśniowej, opartej na przesłankach neurofizjologicznych otrzymanych z rejestracji elektromiograficznych mięśni działających antagonistycznie na stawie nadgarstka i skokowym w obserwacji długoterminowej (po 60 dniach terapii), skojarzonej z usprawnianiem metodą PNF (grupa NMFES+K). Wyniki zostały porównane z rezultatami leczenia głównie z wykorzystaniem PNF (grupa K) u chorych po udarach jako podstawowej metody usprawniania.
REKLAMA

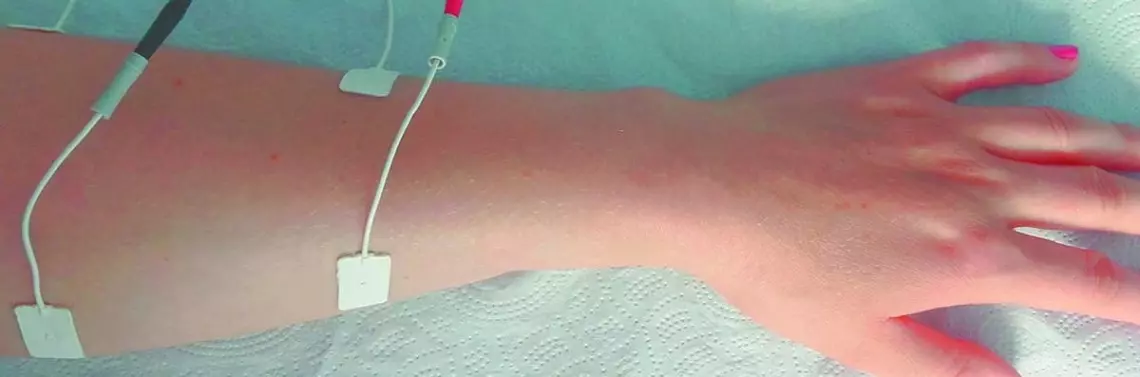
Umiejscowienie par elektrod w trakcie rejestracji sEMG z mięśni prostowników i zginaczy działających antagonistycznie na stawie nadgarstka (A) oraz skokowym (C) w trakcie przykładowej relaksacji (A) oraz maksymalnego skurczu mięśnia piszczelowego przedniego trwającego 5 sekund (C). W B i D pokazano zbliżoną lokalizację par elektrod stymulujących mięśnie działające antagonistycznie kolejno na stawie nadgarstka i skokowym w trakcie sesji elektroterapii.
Metodologia, przeciwwskazania, interpretacja wyników
Badania neurofizjologiczne elektromiografii rejestrującej czynność mięśni elektrodami powierzchniowymi (sEMG) wykonano u 10 zdrowych ochotników grupy kontrolnej oraz u 20 chorych po udarach niedokrwiennych, podzielonych na grupy NMFES+K oraz K, przed terapią (T0) i po 60 dniach terapii (T1) (ryc. 1A i C). Kryterium podziału było pisemne zobowiązanie chorego do przeprowadzania w warunkach domowych zabiegów elektrostymulacji mięśni 3 razy dziennie, 5 razy w tygodniu przez 8 tygodni, po uprzednim instruktażu w warunkach szpitalnych (ryc. 1B i D). Weryfikację częstości przeprowadzanej elektroterapii u chorych umożliwiał odczyt elektroniczny z pamięci stymulatora całkowitej liczby godzin przeprowadzanych sesji terapeutycznych w obserwacji T1.
Kryteriami włączenia chorych do badań były wiek (od 34 do 45 lat), udokumentowane w badaniach MRI oraz badaniach klinicznych skutki niedokrwienia bezpośrednio po incydencie, leczenie na oddziale neurologii, uzyskanie pisemnej zgody chorych na wykonanie badań neurofizjologii klinicznej, wykorzystywanych w pracy, oraz zabiegi spersonalizowanej elektroterapii NMFES i uczestnictwo w sesjach terapeutycznych PNF. Kryteriami wyłączenia z zabiegów elektroterapii NMFES są epizody epilepsji i inne następstwa bezpośrednich urazów czaszkowo-mózgowych, upośledzenie intelektualne, ciąża, implanty o właściwościach ferromagnetycznych, poważne zaburzenia czynności układu sercowo-naczyniowego, implanty elektroniczne (np. rozrusznik serca, wszczep ślimakowy). Na wykonywanie nieinwazyjnych badań oraz zabiegi elektroterapii uzyskano zgodę Komisji Bioetycznej Uniwersytetu Medycznego im. Karola Marcinkowskiego w Poznaniu (Uchwała 1279/18).
Zarówno u zdrowych ochotników grupy kontrolnej, jak i u chorych dwóch grup w obserwacji T0 zostały zarejestrowane metodą sEMG parametry amplitudy (w µV) oraz częstotliwości (w Hz) potencjałów czynnościowych jednostek ruchowych w warunkach całkowitej relaksacji, czynność mięśni w warunkach maksymalnego skurczu, trwająca 5 sekund (wykonywano każdorazowo 3 próby, z których wartości uśredniano), a także czynność naprzemienna mięśni antagonistycznych zginaczy i prostowników nadgarstka oraz stawu skokowego (ryc. 2 i 3). Te same rejestracje powtórzono u chorych obu grup w obserwacji T1 (po około 60 dniach leczenia w warunkach szpitalnych i domowych). Opis analizy i interpretacji wyników badań sEMG w warunkach spoczynkowych i maksymalnego skurczu zamieszczono w innych pracach [10, 11]. Interpretację indeksu sEMG czynności antagonistycznej opisano w pracy Lisińskiego i wsp. [8]: 5 – pełna, prawidłowa czynność naprzemienna, 4 – niepełna czynność naprzemienna, 3 – umiarkowanie nieprawidłowa czynność naprzemienna, 2 – znacząco nieprawidłowa czynność naprzemienna, 1 – brak czynności naprzemiennej.

Zabiegi elektrostymulacji funkcjonalnej NMFES mięśni antagonistycznych działających na stawach nadgarstka oraz skokowym przeprowadzono z wykorzystaniem personalnego, przenośnego, 4-kanałowego aparatu do elektrostymulacji RehaStim4 (Innomed) (ryc. 1B i D). Do aparatu wprowadzano algorytm dostosowanych parametrów bodźców elektrycznych indywidualnie dla usprawnianego chorego (na podstawie wyników przeprowadzonych badań sEMG), z możliwością elektronicznego odczytu z pamięci urządzenia, informującego lekarza i fizjoterapeutę o częstości i regularności jego stosowania, również z możliwością zablokowania parametrów opracowanego algorytmu stymulacyjnego. Algorytm stymulacji zawierał zmiennie: czas trwania jednej sesji stymulacyjnej (2–3 razy dziennie) przez 15–20 minut w zależności od nasilenia zmian w parametrze częstotliwościowym sEMG rejestrowanego w warunkach skurczu maksymalnego (zwykle w zakresie od 40 do 70 Hz), częstotliwość bipolarnych impulsów elektrycznych prostokątnych w aplikowanej serii w zależności od charakteru częstotliwościowego zapisu sEMG rejestrowanego w warunkach skurczu maksymalnego (40–70 Hz), przerwę pomiędzy seriami impulsów – zależną od czasu trwania połowicznego spadku amplitudy sEMG rejestrowanego w warunkach znormalizowanego skurczu maksymalnego trwającego 5 sekund razy 2 (zwykle u chorych po udarze – 4 sekundy), czas trwania pojedynczego impulsu (zwykle od 10 do 15 ms) – zależny od parametru średniego czasu trwania pojedynczych potencjałów czynnościowych jednostek ruchowych rejestrowanych z mięśnia w badaniu sEMG, a także natężenie impulsów stymulujących (zwykle u chorych od 14 do 40 mA).
Porównanie wyników badań neurofizjologicznych rejestrowanych u zdrowych ochotników (N = 10) oraz u chorych po udarach niedokrwiennych, leczonych zabiegami elektrostymulacji funkcjonalnej oraz kinezyterapii (NMFES+K, N = 10) lub wyłącznie zabiegami kinezyterapii (K, N = 10) na dwóch etapach obserwacji (T0 – obserwacja przed terapią, T1 – obserwacja po 60 dniach terapii). Pokazano wartości średnie i odchylenia standardowe lub mediany. W porównaniach różnicę istotną statystycznie przyjęto przy p ≤ 0,05 (zaznaczono pogrubioną czcionką). Objaśnienia: sEMG – elektromiografia rejestrowana elektrodami powierzchniowymi, KKG – kończyny górne, KKD – kończyny dolne, indeks sEMG czynności antagonistycznej: 5 – pełna, prawidłowa czynność naprzemienna, 4 – niepełna czynność naprzemienna, 3 – umiarkowanie nieprawidłowa czynność naprzemienna, 2 – znacząco nieprawidłowa czynność naprzemienna, 1 – brak czynności naprzemiennej.

W tabeli 1 przedstawiono wyniki badań neurofizjologicznych. Parametry amplitud w rejestracjach sEMG w warunkach spoczynkowych, maksymalnego skurczu oraz indeksów sEMG w obserwacji T1 różniły się znacząco od tych, które zostały odnotowane w grupie kontrolnej w odniesieniu do chorych zarówno z grupy NMFES+K, jak i grupy K. Wskazywało to na występowanie objawów zwiększonego napięcia mięśniowego, zwłaszcza w mięśniach zginaczach nadgarstka i mięśniach grupy tylnej goleni, pogorszenie sprawności jednostek ruchowych podczas wysiłku w tych samych grupach mięśniowych i uogólnione zaburzenia regulacji czynności naprzemiennej o charakterze ośrodkowym. Poprawę w postaci zmniejszenia parametru amplitudy sEMG w warunkach relaksacji do wartości około 25 µV (wartość graniczna charakteryzująca prawidłowe napięcie mięśniowe), wzrostu amplitudy rejestracji w warunkach maksymalnego skurczu oraz wzrostu mediany indeksu sEMG stwierdzono w obserwacji T1 głównie u chorych leczonych elektroterapią i zabiegami PNF. Po 60 dniach terapii wyniki badań chorych z grupy NMFES+K nie różniły się znacząco od tych, które rejestrowano u zdrowych ochotników.
Tabela 1. Porównanie wyników badań neurofizjologicznych rejestrowanych u zdrowych ochotników (N=10) oraz u chorych po udarach niedokrwiennych, leczonych zabiegami elektrostymulacji funkcjonalnej oraz kinezyterapii (NMFES+K, N=10) lub wyłącznie zabiegami kinezyterapii (K, N=10) na dwóch etapach obserwacji (T0-obserwacja przed terapią, T1-obserwacja po 60 dniach terapii). Pokazano wartości średnie i odchylenia standardowego lub mediany. W porównaniach różnicę istotną statystycznie przyjęto przy p≤0.05 (zaznaczono pogrubioną czcionką). Objaśnienia: sEMG- elektromiografia rejestrowana elektrodami powierzchniowymi, KKG-kończyny górne, KKD-kończyny dolne, Indeks sEMG czynności antagonistycznej: 5 - pełna, prawidłowa czynność naprzemienna, 4 - niepełna czynność naprzemienna, 3 - umiarkowanie nieprawidłowa czynność naprzemienna, 2 – znacząco nieprawidłowa czynność naprzemienna, 1 – brak czynności naprzemiennej).

Podsumowanie
Przedstawione metody badań neurofizjologicznych umożliwiają obiektywną ocenę dysfunkcji ruchowych u chorych po incydentach mózgowo-naczyniowych oraz definiują nasilenie objawu spastyczności w kończynach niedowładnych przed podjęciem leczenia. Ocena ta może wpłynąć na określenie częstości podejmowanych zabiegów elektrostymulacji i ich czasu trwania. Zaprezentowane wyniki badań sEMG wskazują na uzyskanie lepszego efektu terapeutycznego za pomocą łączonej kinezyterapii i elektrostymulacji funkcjonalnej aniżeli wykorzystanie wyłącznie zabiegów kinezyterapeutycznych u chorych po udarach niedokrwiennych mózgu. Na podstawie wyników tej pracy oraz Lisińskiego i wsp. [10] można wywnioskować, że proponowany, spersonalizowany algorytm elektrostymulacji NMFES daje trwałe i lepsze efekty funkcjonalne aniżeli dotychczas standardowo stosowany, czyniąc go celowanym sposobem leczenia. Czynność naprzemienna mięśni działających na tym samym stawie jest regulowana przez ośrodkowy system rdzeniowy sprzężenia zwrotnego Ia interneuronu hamowania antagonistycznego. U chorych po udarach jest on uwolniony spod kontroli ośrodków nadrdzeniowych, przekazujących wpływy pobudzające i hamujące do interneuronów rdzeniowych zakończeniami aksonów sznurów bocznych rdzenia kręgowego [12]. Znacząca poprawa indeksu sEMG w grupie chorych NMFES+K wskazuje, że ten rodzaj terapii przyczynia się do przywrócenia takiej kontroli.
Piśmiennictwo
- Kabat H., Knott M., Proprioceptive facilitation techniques for treatment of paralysis, „Phys Ther Rev” 1953, 33 (2), s. 53–64.
- Vojta V., Rehabilitation des spastischen infantilen syndroms. Eigene Methodik, „Beitr Orthop Traumat, 1965, 12, s. 557.
- Gajewska E., Huber J., Kulczyk A., Lipiec J., Sobieska M., An Attempt to Explain the Vojta Therapy Mechanism of Action Using the Surface Polyelectromyography in Healthy Subjects: A Pilot Study, „J Bodyw Mov Ther” 2018, 22(2), s. 287–292.
- Quandt F., Hummel F.C., The influence of functional electrical stimulation on hand motor recovery in stroke patients: a review, „Exp Transl Stroke Med” 2014, 6, s. 9.
- Knutson J.S., Fu M.J., Sheffler L.R., Chae J., Neuromuscular Electrical Stimulation for Motor Restoriation in Hemiplegia, „Phys Med Rehabil Clin N Am.” 2015, 26(4), s. 729–745.
- Wolf S.L., Butler A.J., Alberts J.L., Kim M.W., Contemporary linkages between EMG, kinetics and stroke rehabilitation, „J Electromyogr Kinesiol” 2005, 15, s. 229–239.
- Woldag H., Hummelsheim H., Evidence-based physiotherapeutic concepts for improving arm and hand function in stroke patients: a review, „J Neurol” 2002, 249, s. 518–528.
- Lisiński P., Huber J., Samborski W., Witkowska A., Neurophysiological assessment of the electrostimulation procedures used in stroke patients during rehabilitation, „Int. J. Artif. Organs” 2008, 31(1), s. 76–86.
- Kraft G.H., Fitas S.S., Hammond M.C., Techniques to improve function of the arm and hand in chronic hemiplegia, „Arch Phys Med Rehabil” 1992, 73, s. 220–227.
- Lisiński P., Huber J., Evolution of muscles dysfunction from myofascial pain syndrome through cervical disc-root conflict to degenerative spine disease, „Spine” 2017, s. 42(3), s. 151–159.
- Huber J., Lisiński P., Early results of supervised versus unsupervised rehabilitation of patients with cervical pain, „Int J Artif Organs” 2019, 42(12), s. 695–703.
- Baldissera F., Hultborn H., Illert M., Integration in Spinal Neuronal Systems [W:] Handbook of Physiology, The Nervous System, Motor Control, Wyd. Brooks VB, American Physiological Society, Bethesda 1981.